
����Ŀ�����г�����������A��B��C�ͳ�������ס��ҡ���������D��E��F��G��H������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ��������������������Ϣ�ش��������⣺
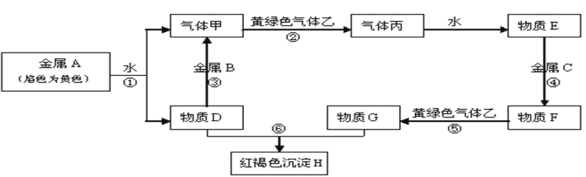
��1��ABC���ֽ����Ļ�ԭ��ǿ����ǿ������˳���ǣ�______________�����þ��廯ѧʽ��ʾ��
��2��д����Ӧ�۵����ӷ���ʽ��__________________________��
��3��ʵ������ȡ������ʱ���Ƚ�����������ͨ�� _____�Գ�ȥ________________��
��4�����ձ���װ�е�����F�м�������D�����Կ����������ǣ�_________������Fͬ��̬�����ӵ�̼�����ڸ�������ʱ��ǿ�ȣ����Եõ���ɫ���壬��Ӧ�Ļ�ѧ����ʽ�ǣ�___��
���𰸡�Na��Al��Fe 2Al+2OH-+2H2O��2AlO2-+3H2�� ����ʳ��ˮ HCl���Ȼ��⣩ ������ɫ�������ɣ�,Ȼ�����̱�ɻ���ɫ,��������ɫ 2FeCO3![]() Fe2O3+CO��+CO2��
Fe2O3+CO��+CO2��
��������
�ɽ���A��ɫ��ӦΪ��ɫ��֪AΪ����Na���ɷ�Ӧ�ٿ�֪��DΪNaOH�������ΪH2���������������B��Ӧ������������BΪ����Al������ɫ������ΪCl2����������Ӧ���ɱ�ΪHCl��HCl����ˮ������EΪ�����������������G��Ӧ���ɺ��ɫ������Fe��OH��3��������G�к���Fe3+����ת����ϵ��֪CΪFe����������FΪFeCl2������GΪFeCl3��
(1) AΪ����Na��BΪ����Al, CΪFe�������ɽ����˳�����֪�����ֽ����Ļ�ԭ��ǿ����ǿ������˳����Na��Al��Fe���ʴ�Ϊ��Na��Al��Fe��
��2����Ӧ��Ϊ������������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�����ӷ���ʽΪ2Al+2OH-+2H2O��2AlO2-+3H2�����ʴ�Ϊ��2Al+2OH-+2H2O��2AlO2-+3H2����
��3��ʵ������Ũ������������̹��ȷ�Ӧ��ȡ������Ũ���������ӷ����Ƶõ������л����Ȼ����ˮ�������Ƚ�����������ͨ��ʢ�б���ʳ��ˮ��ϴ��ƿ�����Գ�ȥ��������ˮ���Ȼ������壬�ʴ�Ϊ������ʳ��ˮ�� HCl���Ȼ��⣩��
��4����װ��ΪFeCl2��Һ�м���NaOH��Һ��NaOH��Һ��FeCl2��Һ��Ӧ���ɰ�ɫ�������������������Ȼ��ƣ������������������ȶ��������е���������Ϊ������������ɫ�������̱�ɻ���ɫ,����ɺ��ɫ������Fͬ��̬�����ӵ�̼����ΪFeCO3���ڸ�������ʱ��ǿ�ȣ��õ���ɫ����ΪFe2O3����ѧ����ʽΪ2FeCO3![]() Fe2O3+CO��+CO2����
Fe2O3+CO��+CO2����
�ʴ�Ϊ�����а�ɫ�������ɣ�,Ȼ�����̱�ɻ���ɫ,����ɺ��ɫ��2FeCO3![]() Fe2O3+CO��+CO2����
Fe2O3+CO��+CO2����


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������칤����м��أ�������ľ��Ϊ�����顢�ܡ������������������ú֡�˿�ࡣ�����е��������顢�ܡ����������ú֡�˿�����ֱ�����
A.��ά�ء���֬B.���ࡢ��֬C.��ά�ء�������D.��֬��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����е������仯����ͼһ�µ���

A. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
B. C+CO2![]() 2CO
2CO
C. CaCO3![]() CaO+CO2��
CaO+CO2��
D. C+H2O![]() CO+H2
CO+H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֱ������Ȼ��Դ�������йؿ�����˵��������ǣ� ��
A.�����ж�����̼����������������ЧӦ��
B.������������Ҫ��Դ��ֲ��Ĺ������
C.��������ָ������Խ�ߣ���������Խ��
D.�����еĵ��������������ԼΪ5��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������½������г���0.8molSO2, 0.2molO2, 0.6molSO3���Ϊ2L���ܱ������У�������Ӧ��2SO2 (g)+ O2 (g)2SO3(g),�ﵽ��ѧ��Ӧ��ʱ��SO3���ʵ��������ǣ��� ��mol
A. 0B. 0.3C. 1.0D. 1.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ,��0.10 mol��L-1�İ�ˮ�ζ�10.00 mL a mol��L-1������,�����Һ��pH�백ˮ�����(V)�Ĺ�ϵ��ͼ��ʾ����֪N����Һ�д���:c(H+)=c(OH-)+c(NH3��H2O),����˵������ȷ����(����)
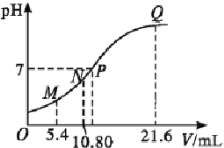
A. ͼ���ĵ����������ͬ
B. a=0.1
C. N��Q�����![]() :N=Q
:N=Q
D. P����Һ�д���:c(Cl-)=c(NH4+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵�����������ࡣ����A��B��C�����ܲ���Ϊ2�ķǽ���Ԫ�ء�������DCΪ���ӻ����D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��AC2Ϊ�Ǽ��Է��ӡ�E�ĺ�������Ų�����6��δ�ɶԵ��ӣ���ͬ���������ģ�ECl3����B��C���⻯���γ��������������������������ʵ���֮��Ϊ2��1������������λ����硣������Ӧ��Ԫ�ط��Ż�ʽ����գ�
��1��д��Ԫ�ص����� A ___________ E ____________��
��2��A��B��C�ĵ�һ��������С�����˳��Ϊ __________��B���⻯����ӵĿռ乹��Ϊ _________ ��
��3��������AC2��һ����B��C��ɵĻ�����X��Ϊ�ȵ����壬��X�Ļ�ѧʽΪ ____________����ȫ��B��ԭ����ɵ�ij������AC2Ҳ���ڵȵ����壬�����ӵĻ�ѧʽΪ _____ ����ռ乹��Ϊ __________ ��
��4��ECl3�γɵ������Ļ�ѧʽΪ ____________________________ ��
��5��D�ĵ�����AC2�п���ȼ�ղ�һ�ְ�ɫ�����һ�ֺ�ɫ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ ________ ��
��6����Eͬ���ڣ������������Ų���ͬ��Ԫ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25�棬101kPa�£�lgC8H18�����飩ȼ�����ɶ�����̼��Һ̬ˮʱ�ų�48.40kJ��������ʾ������Ӧ���Ȼ�ѧ����ʽ��ȷ����( )
A. C8H18��1����12.5O2��g����8CO2��g����9H2O��g�� ��H����48.40kJ��mol��1
B. C8H18��1����12.5O2��g����8CO2��g����9H2O��1�� ��H����5518kJ��mol��1
C. C8H18��1����12.5O2��g����8CO2��g����9H2O��1�� ��H����5518kJ��mol��1
D. C8H18��1����12.5O2��g����8CO2��g����9H2O��1�� ��H����48.40kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H2��ȼ����Ϊ��H����285.8 kJ��mol��1��CO��ȼ����Ϊ��H����282.8 kJ��mol��1������H2��CO��ɵĻ������5.6 L(��״��)�������ȼ�պų�������Ϊ71.15 kJ��������Һ̬ˮ������˵����ȷ����
A. COȼ�յ��Ȼ�ѧ����ʽΪ2CO(g)��O2(g)===2CO2(g)����H����282.8 kJ��mol��1
B. H2ȼ�յ��Ȼ�ѧ����ʽΪ2H2(g)��O2(g)===2H2O(g)����H����571.6 kJ��mol��1
C. ȼ��ǰ���������CO���������Ϊ60%
D. ȼ�պ�IJ���ȫ���������Ĺ����������ÿɲ���0.125 mol O2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com