
【题目】下列浓度关系正确的是( )
A.向0.1mol/LNH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全:c(NH4+)>c(OH-)>c(SO42-)>c(H+)
B.向0.1mol/L的KOH溶液中通入标准状况下的CO2气体3.36L,所得溶液中:c(K+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
C.pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c(NaOH)<c(CH3COONa)<c(NaHCO3)<c(Na2CO3)
D.0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液呈碱性:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+)
【答案】D
【解析】
A. 向0.1mol/LNH4HSO4溶液中滴加0.1mol/L的Ba(OH)2溶液至沉淀刚好完全,此时所用二者的体积刚好相同,生成BaSO4、NH3·H2O,溶液中主要发生NH3·H2O和H2O的电离,溶液中离子浓度关系为c(OH-)> c(NH![]() ),A错误;
),A错误;
B. 向0.1mol/L的KOH溶液中通入标准状况下的CO2气体3.36L,虽然不能确定生成何种物质,但 “c(K+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)”违背电荷守恒原则,所以B错误;
C. 因为电离能力CH3COOH>H2CO3>HCO3-,所以要产生相同浓度的OH-,应有下列关系:c(CH3COONa)>c(NaHCO3)>c(Na2CO3),NaOH完全电离出OH-,所需浓度最小,从而得出pH相同的NaOH溶液、CH3COONa溶液、Na2CO3溶液、NaHCO3溶液的浓度:c(NaOH)<c(Na2CO3)<c(NaHCO3)<c(CH3COONa),C错误;
D. 0.1mol/L的NaOH溶液与0.2mol/L的HCN溶液等体积混合,所得溶液中,
c(HCN)=0.05mol/L,c(NaCN)=0.05mol/L,因为溶液呈碱性,所以主要发生以下反应:
CN-+H2O![]() HCN+OH-,H2O
HCN+OH-,H2O![]() H++OH-,从而得出:c(HCN) >c(Na+)>c(CN-)>c(OH-)>c(H+),D正确。
H++OH-,从而得出:c(HCN) >c(Na+)>c(CN-)>c(OH-)>c(H+),D正确。
故选D。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】化合物A由三种元素组成,某兴趣小组进行了如下实验:

已知:气体甲为纯净物且只含两种元素,在标况下体积为672 mL;溶液乙为建筑行业中常用的粘合剂。
请回答下列问题:
(1)A的组成元素为________(用元素符号表示);
(2)写出气体甲与NaOH(aq)反应的离子方程式________;
(3)高温下,A与足量氯气能发生剧烈爆炸,生成三种常见化合物试写出相应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X由三种元素组成,为探究其组成的性质,设计并完成如下实验:
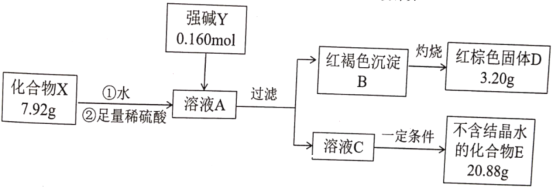
提示:化合物E的焰色反应为紫色(透过蓝色钴玻璃)
请回答:
(1)X的化学式是________________。强碱Y的电子式为________________。
(2)在常温和干燥的条件下,化合物X可以稳定存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀和一种气体单质。
①化合物X与水反应的离子方程式为________________。
②人们针对化合物X的稳定性进行了大量的研究,并取得了一定的进展。下列物质可以提高化合物X在水溶液中稳定性的是________________。
A KHSO4 B K2CO3 C CH3COOK D K2SO3
③为研究温度对化合物X水溶液稳定性的影响,请设计一个实验方案:________________________________________________。
(3)化合物X有多种制备方法其中一种方法是在强碱Y条件下用次氯酸钾与红褐色沉淀B反应,其化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是( )
A.1 L 0.1 mol·![]() NH4Cl溶液中,NH4+的数量为0.1NA
NH4Cl溶液中,NH4+的数量为0.1NA
B.2.4g镁在足量的O2中燃烧,转移的电子数为0.1NA
C.标准状况下,5.6 L CO2气体中含有的氧原子数为0.5NA
D.1 mol N2与3 mol H2反应生成的NH3分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:2SO3(g)![]() 2SO2(g)+O2(g)△H=+197kJ/mol。实验测得起始、平衡时的有关数据如下表:
2SO2(g)+O2(g)△H=+197kJ/mol。实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物 质 的量 /mol | 平衡时反应中的能量变化 | ||
SO3 | SO2 | O2 | ||
① | 2 | 0 | 0 | 吸收热量akJ |
② | 0 | 2 | 1 | 放出热 量 bkJ |
③ | 4 | 0 | 0 | 吸收热量ckJ |
下列叙述正确的是( )
A. 达平衡时O2的体积分数:①>③
B. 热量关系:a一定等于b
C. ①②③ 反应的平衡常数:③>①>②
D. ①中的密度不再改变时说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、N的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y的次外层电子数是其电子总数的1/4,离子化合物ZX2是一种储氢材料,W与Y属于同一主族,NY2是医学上常用的水消毒剂、漂白剂。下列叙述正确的是 ( )
A.Y和W分别与X形成的简单化合物的热稳定性:X2 Y > X2W
B.离子半径由大到小的顺序为Y2-< Z2+< N-< W2-
C.ZX2和NY2中含有化学键一致,且微粒个数之比均为1 : 2
D.含氧酸的酸性N > W,可证明非金属性:N > W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有八种物质:①甲烷、②苯、③聚丙烯、④聚异戊二烯、⑤2一丁炔、⑥环己烷 ⑦邻二甲苯⑧裂解气,既能使酸性KMnO4溶液褪色又能与溴水反应使之褪色的是( )
A.③④⑤⑦⑧B.④⑤⑧C.④⑤⑦⑧D.③④⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O是黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。制取Cl2O的装置如图所示。

已知:Cl2O的熔点为-116 ℃,沸点为3.8 ℃,Cl2O在空气中的百分含量达到25%以上易爆炸;Cl2的沸点为-34.6 ℃;HgO+2Cl2==HgCl2+Cl2O。下列说法中不正确的是
A.装置②③中盛装的试剂依次是饱和食盐水和浓硫酸
B.通入干燥空气的目的是将生成的Cl2O稀释,减小爆炸危险
C.从装置⑤中逸出气体的主要成分是Cl2O
D.装置④与⑤之间不用橡胶管连接,是为了防止橡胶管燃烧和爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若20g密度为ρg·cm-3的Ca(NO3)2溶液中含有2gCa(NO3)2,则溶液中![]() 的物质的量浓度为
的物质的量浓度为
A.![]() mol·L-1B.
mol·L-1B.![]() mol·L-1C.
mol·L-1C.![]() mol·L-1D.
mol·L-1D.![]() mol·L-1
mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com