
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了 腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了 (“氧化”或“还原”)反应,其电极反应式是 。
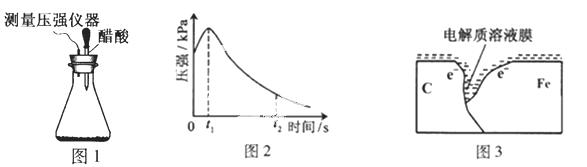
(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二: ;
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案。请你再设计一个实验方案验证假设一,写出实验步骤和结论。
| 实验步骤和结论(不要求写具体操作过程): |
科目:高中化学 来源: 题型:
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,产物有HF、NO和HNO3。下列关于该反应的说法中,正确的是( )
A.水蒸气在反应中被NF3氧化
B.反应中氧化产物与还原产物的物质的量之比为1:2
C.反应中生成22. 4 L NO气体时,转移电子的物质的量为1 mol
D.NF3在空气中泄漏时没有明 显现象,用石灰水溶液喷淋的方法可减少污染
显现象,用石灰水溶液喷淋的方法可减少污染
查看答案和解析>>
科目:高中化学 来源: 题型:
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
 (1)A的分子式为 :
(1)A的分子式为 :
 (2)A与溴的四氯化碳溶液反应的化学方程式为 ,反应类型是 ;
(2)A与溴的四氯化碳溶液反应的化学方程式为 ,反应类型是 ;
 (3)已知:
(3)已知: 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
 (4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 ;
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 ;
 (5)在一定条件下,由A聚合得到的高分子化合物的结构简式为 。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.铁的应用经历了“铁—普通钢—不锈钢等特种钢”的演变过程
B.减少生铁里的碳元素,并增加硅、锰等元素,即转化为钢
C.普通钢中的含铬量一般在12%以上
D.不锈钢是在普通钢的基础上,加入铬、镍等多种元素炼成的钢材
查看答案和解析>>
科目:高中化学 来源: 题型:
1)已知Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下(所取溶液体积均为10 mL):
| 实验编号 | 实验温度/℃ | c(Na2S2O3) /mol·L-1 | c(H2SO4) /mol·L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
其他条件不变时,探究温度对化学反应速率的影响,应选择__________(填实验编号);探究浓度对化学反应速率的影响,应选择__________(填实验编号);若同时选择①②③溶液变浑浊的同时,探究__________对化学反应速率的影响。
(2)已知Na2S2O3溶液与Cl2反应时,1 mol Na2S2O3转移8 mol电子。该反应的离子方程式是____________________________________________________________,
甲同学设计如下实验流程探究Na2S2O 3的化学性质。
3的化学性质。
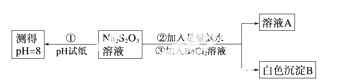
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和________性。
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是________________________。
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是________(填“甲”或“乙”),理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为 ,若有3mol FeS2参加反应,转移 mol电子。
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程式表示)。
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有无色气体逸出,请写出相应的离子方程式: 。
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL 5mol•L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),往反应后溶液中滴加KSCN溶液,无明显现象,则参加反应的铁粉的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能大量共存的是( )
|
| A. | Fe3+、SCN﹣、Na+、Cl﹣ | B. | Cl﹣、AlO2﹣、HCO3﹣、Na+ |
|
| C. | Fe2+、NH4+、SO42﹣、S2﹣ | D. | Ca2+、HCO3﹣、Cl﹣、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据实验目的判断下列实验操作或装置正确的是
| 目的 | A.检验火柴头燃烧 产生的SO2 | B.配制稀硫酸 溶液 | C.分离Cl2与KBr 反应生成的Br2 | D.检查装置 气密性 |
| 装置 或 操作 |
|
|
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com