
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是
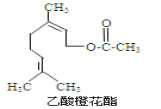
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
A.①②③ B.①②⑤ C.①②⑤⑥ D.①②④⑤
科目:高中化学 来源: 题型:
【题目】乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为 ;
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸 碳酸(填“>”或“<”);
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+ 。
CH3COOCH2CH3+ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表中的一部分。用化学式或元素符号回答下列问题:
IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10种元素中,化学性质最不活泼的是__________(填元素名称)。
(2)三周期元素除⑩外原子半径最小的是______(填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是__________(填化学式,下同),具有两性的是____________。
(3)在室温下有颜色的气体单质溶于水的离子方程式为_____ __;
(4)⑧与⑨分别与H2形成的氢化物的稳定性:__________,(用化学式表示)最高价氧化物对应的水溶液的酸性由强到弱的顺序:______ _________。(用化学式)
(5)①③⑤单质的活泼性顺序为_____>____>____(填元素符号),判断的实验依据是__(写出一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
X、Y、Z、W、Q为前四周期的五种元素,且原子序数依次增大。已知X、Y、Z、W均为非金属元素,XW2分子与Y3-为等电子体,元素W和元素Z为同族元素,Q的最外层电子数为2,次外层电子数等于Y和W2 -最外层电子数之和,根据以上信息回答下列问题:
(1)上述五种元素中电负性最大的是___(填元素符号,下同),Y的第一电离能大于Z的第一电离能原因___________________________________。
(2)XW2的电子式为______________。
(3)Q的价电子排布式为_____________,Y3-的分子构型为______________。
(4)下列关于WZ2结构的说法正确的是___________(填序号)。
a.WZ2为直线形非极性分子 b.WZ2为直线形极性分子
c.WZ2中W为sp3杂化 d.WZ2中W为sp2杂化
(5) W有两种常见的含氧酸,较高价的酸性比较低价的______,理由______________。
(6)α-QW的晶胞是立方体,用X射线衍射法测得该晶体晶胞边长=520.0pm,26℃测得该晶体的密度为4.1g/cm3,请列式计算一个晶胞中含有的Q、W离子数。(5.23≈140.6)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】、近年来,我国的雾霾问题引起政府和群众的高度关切,一般认为细颗粒物(即PM2.5,指直径小于或等于2.5微米的颗粒物)的指标与雾霾天气密切相关。与此同时,光化学烟雾也开始抬头,它是由非甲烷烃和NOx的排放引起的,严重时天空会出现彩色云雾,属于一种重污染现象。臭氧浓度升高是光化学烟雾形成的标志。请回答下列相关问题:
(1)以下可能引起细颗粒物指标变高的是 (填序号)。
a.燃煤取暖 b.大型交通设备 c.生活污水 d.火山喷发 e.局部战争 f.采矿业
(2)下图是某地光化学烟雾的日变化曲线:据图所示,

上午8:00,非甲烷烃和NO出现峰值。 随后NO2约于10:00达峰值,其主要反应的方程式可能为 。8:00起,O3开始积累,并于13:00达峰值,O3积累与下列过程有关: O+O2 →O3,该反应物中游离的氧原子主要是由反应: 产生的。O3又使10:00前NO2的含量急剧增加,其化学方程式为 。你认为该地光化学烟雾较严重的时间最可能为 (填序号)。
a.8:00 b.10:00 c.15:00 d.20:00
(3)若25℃、101kPa下,气体的摩尔体积为24.5L/mol,此条件下向容器中充入一定量N2O4,当NO2 与N2O4的平衡混合物密度为3.18 g/L时,混合气体的平均摩尔质量为 ,N2O4的分解率(即转化率)为 。(计算结果均保留三位有效数字)。
(4)NO、NO2、NH4+及NO2-等被称为活性氮物质,超量排放会引起环境问题。NH4+与NO2-可发生下列反应:NH4+(aq)+NO2-(aq) ![]() N2(g)+2H2O(l)可加快该反应的措施为 。该反应的反应速率方程为ν = k·c(NH4+)x·c(NO2-)y,其中k为速率常数,在一定温度下,进行下列实验:
N2(g)+2H2O(l)可加快该反应的措施为 。该反应的反应速率方程为ν = k·c(NH4+)x·c(NO2-)y,其中k为速率常数,在一定温度下,进行下列实验:
实验序号 | c(NH4+)/mol·L-1 | c(NO2-)/mol·L-1 | ν/ mol·L-1·s-1 |
1 | 0.0100 | 0.200 | 5.4×10-7 |
2 | 0.0200 | 0.200 | 1.08×10-6 |
3 | 0.200 | 0.040 | 2.16×10-6 |
4 | 0.200 | 0.060 | 3.24×10-6 |
据表知,将溶液稀释至原体积的2倍,反应速度将变为原来的 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料的使用和防污染是社会发展中一个无法回避的矛盾话题。
(1)我国北方冬季烧煤供暖所产生的废气是雾霾的主要来源之一。经研究发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g)═N2(g)+2CO2(g) △H
若①N2(g)+O2(g)═2NO(g) △H1=+180.5 kJ·mol-1
②CO(g)═C(s)+![]() O2(g) △H2=+110.5 kJ·mol-1
O2(g) △H2=+110.5 kJ·mol-1
③C(s)+O2(g)═CO2(g) △H3=﹣393.5 kJ·mol-1
则△H= kJ·mol-1.
(2)甲醇可以补充和部分替代石油燃料,缓解能源紧张。一定条件下,在容积为VL的密闭容器中充入a molCO与2a mol H2合成甲醇,CO平衡转化率与温度、压强的关系如图所示。
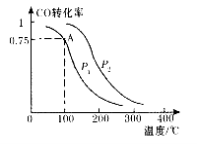
①P1_ P2(填“>” 、“<” 或“=” ),理由是
②该甲醇合成反应在A点的平衡常数K= (用a和V表示)。
③下列措施中能够同时满足增大反应速率和提高CO转化率的是 。(填写相应字母)
a、使用高效催化剂 b、降低反应温度 c、增大体系压强
d、不断将CH3OH从反应混合物中分离出来 e、增加等物质的量的CO和H2
(3)机动车的尾气也是雾霾形成的原因之一。

①近几年有人提出在催化剂条件下,利用汽油中挥发出来的C3H6催化还原尾气中的NO气体生成三种无污染的物质。请写出该过程的化学方程式: 。
②电化学气敏传感器法是测定汽车尾气常用的方法之一。其中CO传感器的工作原理如上图所示,则工作电极的反应式为 。
(4)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是 ,用文字和化学用语解释原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种前四周期的元素。A原子核外有1个未成对电子,A+比B原子少一个电子层,B原子得一个电子填入3p轨道后,3p轨道呈全充满状态。C原子的2p轨道有2个未成对电子,D的最高化合价和最低化合价的代数和为4,与C的核电荷数相差8。E位于周期表第12纵列且是六种元素中原子序数最大的。R是由D、E形成的化合物,其晶胞结构如图所示。请回答下列问题:
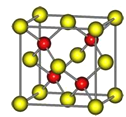
(1)C元素的电负性___D元素的电负性(填“>”、“<”或“=”)。
(2)C的第一电离能比它同周期前一族相邻元素的第一电离能________
(填“大”或“小”)。
(3)E的价电子排布式为_______ _,该元素位于周期表中__ _族。
(4)化合物A2D的电子式为______________________。
(5)D和B形成的一种化合物D2B2广泛用于橡胶工业,它的分子结构与双氧水相似,但在该化合物分子中,所有原子最外层均满足8电子稳定结构。则D2B2分子中D原子的杂化类型是__________,D2B2是_________分子(填“极性”或“非极性”)。
(6)R的化学式为________________(用元素符号表示)。已知R晶体的密度为ρ g·cm-3,则该晶胞的边长a=_____________ cm,(阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:

(1)A的分子式是C7H8,其结构简式是___________________。
(2)试剂a是_______________。① ③ ② ④ ⑤ ⑥ n
(3)反应③的化学方程式:_______________。
(4)E的分子式是C6H10O2。E中含有的官能团:_______________。
(5)反应④的反应类型是_______________。
(6)反应⑤的化学方程式:_______________。
(5)已知: 。
。
以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是利用盐桥电池从某些含碘盐中提取碘的两个装置, 下列说法中正确的是

A.两个装置中石墨I和石墨II作负极
B.碘元素在装置①中被氧化,在装置②中被还原
C.①中MnO2的电极反应式为:MnO2+2H2O+2e-==Mn2++4OH
D.反应①、②中生成等量的I2时导线上通过的电子数之比为1∶5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com