
关于下列各图的叙述,正确的是( )
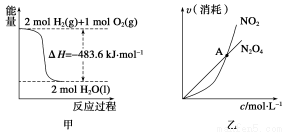
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ·mol-1
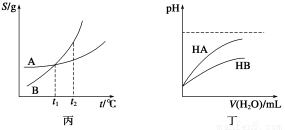
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1 ℃升温至t2 ℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液的pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:2014年高考化学 题型四 离子反应型专题练习卷(解析版) 题型:选择题
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
选项离子组加入试剂加入试剂后发生反应的离子方程式
ANH4+、Fe2+、SO42-少量Ba(OH)2溶液2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3·H2O
BMg2+、HCO3-、Cl-过量NaOH溶液Mg2++2HCO3-+4OH-=2H2O+Mg(OH)2↓+2CO32-
CK+、NH3·H2O、CO32-通入少量CO22OH-+CO2=CO32-+H2O
DFe2+、NO3-、HSO3-NaHSO4溶液HSO3-+H+=SO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十三 表格实验型专题练习卷(解析版) 题型:选择题
下列实验操作正确且能达到预期目的的是( )
| 实验目的 | 操作 |
① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
② | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
③ | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
④ | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
⑤ | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
⑥ | 确定碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO3水溶液的pH |
A.①④⑤ B.②③⑤ C.①⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十一 图像分析型专题练习卷(解析版) 题型:选择题
下列关于甲、乙、丙、丁四个图像的说法中,正确的是( )

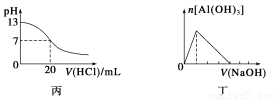
A.图甲表示向乙酸溶液中通入NH3过程中溶液导电性的变化
B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右
C.图丙表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化
D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十 粒子变化型专题练习卷(解析版) 题型:选择题
在25 ℃时,将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液,若此溶液中c(CH3COO-)>c(Cl-),则下列判断不正确的是( )
A.该溶液的pH小于7
B.c(CH3COOH)+c(CH3COO-)=0.20 mol·L-1
C.c(CH3COOH)<c(CH3COO-)
D.c(CH3COO-)+c(OH-)=0.10 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十 粒子变化型专题练习卷(解析版) 题型:选择题
在0.1 mol·L-1的NH4HSO4溶液中,下列微粒的物质的量浓度关系不正确的是 ( )
A.c(H+)>c(SO42-)>c(NH4+)
B.c(NH4+)+c(H+)=2c(SO42-)+c(OH-)
C.c(H+)=c(NH4+)+c(NH3·H2O)+c(OH-)
D.室温下滴加NaOH溶液至中性后:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型八 能量变化型专题练习卷(解析版) 题型:选择题
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图。下列说法正确的是( )
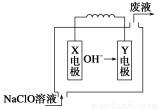
A.镁作Y电极
B.电池工作时,Na+向负极移动
C.废液的pH大于NaClO溶液的pH
D.X电极上发生的反应为ClO-+2H2O-4e-=ClO3-+4H+
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型九 速率平衡型专题练习卷(解析版) 题型:选择题
一定温度下,在2 L密闭容器中发生下列反应:4NO2(g)+O2(g) 2N2O5(g);已知该反应的平衡常数:K300 ℃>K350 ℃,且n(NO2)(单位:mol)随时间变化如下表:
2N2O5(g);已知该反应的平衡常数:K300 ℃>K350 ℃,且n(NO2)(单位:mol)随时间变化如下表:
时间(s) | 0 | 500 | 1000 | 1500 |
t1℃ | 20 | 13.96 | 10.08 | 10.08 |
t2℃ | 20 | a | b | c |
下列说法一定正确的是( )
A.正反应为吸热反应
B.如果t2℃<t1℃,那么a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1 000 s至1 500 s之间
D.如果t2℃>t1℃,那么b>10.08
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com