
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层
电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙是由X、Y、Z组成的盐。下列说法正
确的是 ( )
A.原子半径:W>Y>Z,简单离子半径: Y>Z>W
B.YX 3的空间构型是三角锥型,而Y2X4的空间构型类似于乙烯的空间构型
C.测得乙的水溶液呈酸性,则溶液中乙盐阳离子浓度大于酸根离子浓度
D. W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
有0.4 g铁的氧化物用足量的CO在高温下将其还原,把生成的全部CO2通入足量澄清石灰水中,得到
0.75 g固体沉淀物。这种铁的氧化物的化学式为( )
A.FeO B.Fe2O3 C.Fe3O4 D.FeO、Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
在FeCl3和CuCl2的混合溶液中加入铁屑,反应结束后滤出固体物质,滤液中的阳离子可能是 ( )
①只有Fe2+ ②Fe2+和Fe3+
③Fe2+和Cu2+ ④Cu2+和Fe3+
A.①③ B.②④ C.①④  D.②③
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
向5 mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag2S B.AgCl<AgI<Ag2S
C.AgCl>AgI>Ag2S D.AgI>AgCl>Ag2S
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶电解质在水溶液中存在溶解平衡:
MmAn(s)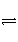
 mMn+(aq)+nAm-(aq)
mMn+(aq)+nAm-(aq)
Ksp=[Mn+]m·[Am-]n,称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)
| 难溶电 解质 | CaCO3 | CaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 mol-2·L-2 | 9.1×10-6 mol-2·L-2 | 6.8×10-6 mol-2·L-2 | 1.8×10-12 mol-3·L-3 |
实验步骤如下:
①往100 mL 0.1 mol·L-1的CaCl2溶液中加入100 mL 0.1 mol·L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液。
④________________________________________________________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(3)设计第③步的目的是
________________________________________________________________________。
(4)请补充第④步操作及发生的现象:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
香花石被誉为“矿石熊猫”,由我国地质
学家首次发现,它由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,
Z的最外层电子数与次外层相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的
3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是: ( )
A.原子半径:Y>Z>R>T B.气态氢化物的稳定性:W<R<T
C.最高价氧化物对应的水化物碱性:X>Z D.XR2、WR2两化合物中R的化合价相同
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ的热量,下列热化学方程式正确的是 ( )
A.H2O(g)=H2(g)+O2(g); ΔH=+242 kJ·mol-1
B.2H2(g)+O2(g)=2H2O(l); ΔH=-484 kJ·mol-1
C.H2(g)+ O2(g)=H2O(g); ΔH=+242 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g); ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下表给出几种氯化物的熔、沸点:
| NaCl | MgCl2 | CaCl2 | SiCl4 | |
| 熔点(℃) | 801 | 712 | 782 | -68 |
| 沸点(℃) | 1 465 | 1 412 | 1 600 | 57.6 |
则下列各项中与表中数据一致的有( )
①CaCl2属于离子晶体 ②SiCl4是分子晶体 ③1 500 ℃时,NaCl可气化 ④MgCl2水溶液不能导电
A.仅① B.仅②
C.①②④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com