
| A. | 煤的干馏是物理变化 | |
| B. | 液化石油气和天然气的主要成分都是碳氢化合物 | |
| C. | 石油裂化得到的汽油是纯净物 | |
| D. | 煤的气化和石油的分馏都是物理变化 |
分析 A、煤的干馏是将煤隔绝空气加强热使煤分解的过程;
B、液化石油气和天然气的主要成分都是烃;
C、汽油是多种烃的混合物;
D、煤的气化是化学变化.
解答 解:A、煤的干馏是将煤隔绝空气加强热使煤分解获得煤焦油、焦炉煤气和粗氨水的过程,是化学变化,故A错误;
B、液化石油气是碳原子数在C3-C4的烃类,天然气的主要成分是甲烷,均是烃类,都是碳氢化合物,故B正确;
C、无论是裂化汽油还是直馏汽油均是多种烃的混合物,故C错误;
D、煤的气化是将煤在高温条件下和水蒸气反应生成CO和氢气的过程,是化学变化,故D错误.
故选B.
点评 本题考查了煤和石油的综合利用,难度不大,应注意的是煤的干馏是化学变化,而石油的分馏是物理变化.


科目:高中化学 来源: 题型:选择题
| A. | 由极性键构成的极性分子 | B. | 由极性键构成的非极性分子 | ||
| C. | 由非极性键构成的极性分子 | D. | CO2中C采取sp2杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A2和B2的总能量之和大于生成的2AB的总能量,则反应放热 | |
| B. | 若A2和B2的总能量之和小于生成的2AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2<Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2<Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
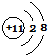 .D在周期表中位置第三周期第ⅥA族.
.D在周期表中位置第三周期第ⅥA族.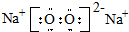 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CCl4>CHCl3>H2O>苯 | |
| C. | 含氢质量分数:甲烷>乙烷>乙烯>乙炔>苯 | |
| D. | 同物质的量的物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 的名称为3,3,6-三甲基辛烷;
的名称为3,3,6-三甲基辛烷;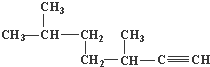 的名称为3,6-二甲基-1-庚炔;
的名称为3,6-二甲基-1-庚炔; ;
;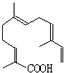 所示,分子式为C15H22O2;该物质可以与下列ABCD(填序号)发生反应.
所示,分子式为C15H22O2;该物质可以与下列ABCD(填序号)发生反应. 中含有的官能团的名称为羟基,酯基.
中含有的官能团的名称为羟基,酯基. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 所加试剂(填化学式) | 离子方程式 |
| ①Mg(OH)2(Al(OH)3) | ||
| ②NaHCO3溶液(Na2CO3) | ||
| ③FeCl2溶液(FeCl3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
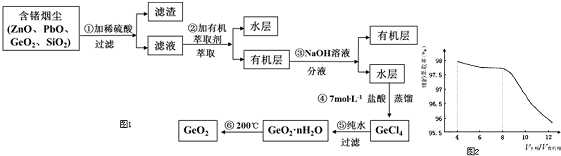
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com