
【题目】等物质的量的SO2和SO3相比较,下列结论错误的是( )
A.它们的分子数目之比是1:1
B.它们的氧原子数目之比为2:3
C.它们的质量之比为1:1
D.它们所含原子数目之比为3:4
【答案】C
【解析】A、等物质的量的SO2和SO3分子数目之比等于物质的量之比=1:1,A不符合题意;
B、等物质的量的SO2和SO3分子数目之比等于物质的量之比=1:1,1个SO2分子中含有2个氧原子,1个SO3分子中含有3个氧原子,则所含O原子数之比为(1×2):(1×3)=2:3,B不符合题意;
C、等物质的量的SO2和SO3质量之比等于物质的摩尔质量之比=64:80=4:5,C符合题意;
D、等物质的量的SO2和SO3分子数目之比等于物质的量之比=1:1,1个SO2分子中含有3个原子,1个SO3分子中含有4个原子,则原子总数之比为(1×3):(1×4)=3:4,D不符合题意;
故答案为:C
A.根据公式![]() 判断,分子数目之比等于物质的量之比;
判断,分子数目之比等于物质的量之比;
B.原子数目之比,应结合化学式中原子个数判断;
C.根据公式![]() 判断,物质的量相等时,质量之比等于摩尔质量之比;
判断,物质的量相等时,质量之比等于摩尔质量之比;
D..原子数目之比,应结合化学式中原子个数判断。


科目:高中化学 来源: 题型:
【题目】配制350mL1.0mol/LH2SO4溶液,需用98%的浓硫酸溶液(ρ=1.84g/L)体积为多少?取25mL1.0mol/LH2SO4溶液与2g锌粉充分反应,产生标准状况下H2多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的方案可以降低铁闸门的腐蚀速率.下列判断正确的是( )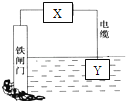
A.若X为导线,Y可以是锌
B.若X为导线,铁闸门上的电极反应式为Fe﹣2e→Fe2+
C.若X为直流电源,铁闸门做负极
D.若X为直流电源,Y极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2molCO(NH2)2中含_____mol碳原子,_____mol氧原子,_____mol氮原子,____mol氢原子,所含氧原子数跟_____molH2O中所含氧原子数相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能减慢化学反应速率的是
A. 用Zn和2mol·L-1H2SO4反应制取H2时,向溶液中滴加少量CuSO4溶液
B. 日常生活中,将食物贮藏在冰箱中
C. 用过氧化氢溶液制氧气时添加少量二氧化锰粉末
D. 用相同质量的锌粉替代锌粒与同浓度、同体积的盐酸反应制氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体.相应的实验过程如图:
(1)写出实验过程中所用试剂(写化学式):
试剂①;试剂③ .
(2)判断试剂①已过量的方法是: .
(3)用离子方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯.
操作①的实验结果:淀粉(填“能”或“不能”)透过半透膜;SO42﹣(填“能”或“不能”)透过半透膜.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物结构、性质相关的叙述中,正确的是( )
A.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的变化过程,上述两个反应属于水解反应
B.丹参素结构如图 ![]() 所示,能发生取代、加成、氧化反应
所示,能发生取代、加成、氧化反应
C.乙烯含双键,可使酸性KMnO4溶液褪色,而乙醇中只含单键不能使酸性高锰酸钾溶液褪色
D.回收地沟油,水解制氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的两个实验装置,溶液的体积均为200mL.开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液和体积变化,下列叙述中正确的是( )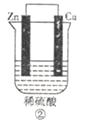
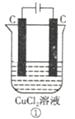
A.产生气体的体积:①>②
B.溶液的pH变化:①减小,②增大
C.电极上生成物质的质量:①=②
D.电极反应式:①中阳极2Cl﹣﹣2e﹣═Cl2↑,②中负极2H++2e﹣═H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】验证某有机物属于烃的含氧衍生物,应完成的内容是
A. 只要验证它完全燃烧后产物只有H2O和CO2
B. 只要测定其燃烧产物中H2O和CO2物质的量的比值
C. 测定完全燃烧时消耗有机物与生成H2O和CO2的物质的量之比
D. 测定该试样的质量及其试样完全燃烧后生成H2O和CO2的质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com