
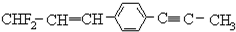 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )| A. | 12个碳原子不可能都在同一平面上 | |
| B. | 处于同一直线上的原子最多有4个 | |
| C. | 处在同一平面上的原子最多有20个 | |
| D. | 除苯环外的其余碳原子有可能都在同一直线上 |
分析 根据常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转.
解答 解:A. 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面,故A错误;
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面,故A错误;
B.乙炔为直线形分子,其中两个C处于一条直线上,苯环上两个碳与其共直线,另外乙烯为平面分子,乙烯的两个碳可以与苯环共直线,故处于同一直线上的原子多于4个,故B错误;
C. 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子(或一个氟原子)共平面,则两个甲基有2个氢原子(或一个氟原子)可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故C正确;
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子(或一个氟原子)共平面,则两个甲基有2个氢原子(或一个氟原子)可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故C正确;
D.乙烯是平面结构,不是直线结构,其余碳原子不可能都在一条直线上,故D错误,故选C.
点评 本题考查有机物结构中共面、共线问题,难度中等,关键是空间想象,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,单键可以旋转.


科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①②③ | C. | ②③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中溶解性 |
| 正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
| 正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
| 溴化氢 | 81 | --- | --- | 极易溶解 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
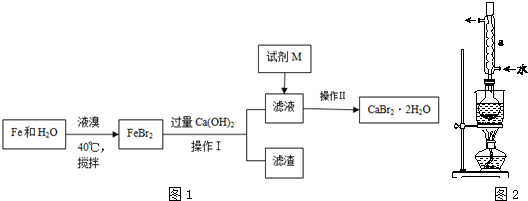
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M为H2O | |
| B. | 每还原1 mol氧化剂,就有3 mol电子转移 | |
| C. | 还原性:SnCl2>As | |
| D. | 氧化产物和还原产物的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2或SO2都会导致酸雨的形成 | |
| B. | 苯与溴水在铁催化下可发生取代反应 | |
| C. | 生铁中含有碳,抗腐蚀能力比纯铁弱 | |
| D. | 电解水生成H2和O2的实验中,可加入少量盐酸增强导电性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.8×10-3mol | B. | 4.4×10-3mol | C. | 3.2×10-3mol | D. | 2.2×10-3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
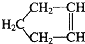 可简写为
可简写为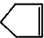 降冰片烯的分子结构可表示为:
降冰片烯的分子结构可表示为: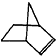
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com