
| ��� | ��Ӧ�¶�/�� | c��H2O2��/mol•L-1 | V��H2O2��/mL | m��MnO2��/g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
���� ��1���������ݲ�ͬ�����ʵ��Ŀ�ģ����ݱ�������֪��ʵ��2��ʵ��3��Ҫ��˫��ˮ��Ũ�Ȳ�ͬ��
��2��̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��ʱ��Ӧ��ֻ���¶Ȳ�ͬ������������ȫ��ͬ��
��3������1��ʵ��2��Ƚϣ�2��ʹ���˴���������������ͬ��
��4������0.1mol•L-1 KSCN��Һ�������Һ����Ѫ��ɫ��˵����Һ����û��Ӧ��FeCl3��Һ��˵���˷�ӦΪ���淴Ӧ��
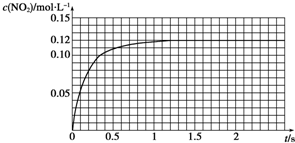
����ΪN2O4��g��?2NO2Ϊ���淴Ӧ����Ӧ��ƽ��ʱ����Ӧ���������ʣ���������NO2��N2O4���ٸ���ƽ��ͼ�����N2O4�����ʵ�����
��v��NO2��=$\frac{��c}{��t}$��
��� �⣺��1��ʵ��2��ʵ��3��ֻ��˫��ˮŨ�Ȳ�ͬ������������ȫ��ͬ������ʵ��Ŀ����̽��˫��ˮŨ�ȶԻ�ѧ��Ӧ����Ӱ�죬�ʴ�Ϊ��H2O2��Ũ�ȣ�
��2��Ҫ̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬Ӧ��ֻ���¶Ȳ�ͬ������������ȫ��ͬ�����ݱ�������֪��ʵ��2��ʵ��4���¶Ȳ�ͬ����������ͬ���ʴ�Ϊ��2��4��
��3������1��ʵ��2��Ƚϣ�2��ʹ���˴���������������ͬ�������ӿ췴Ӧ���ʣ����̷�Ӧ�ﵽƽ��ʱ�䣬����t1��t2���ʴ�Ϊ������
��4������0.1mol•L-1 KSCN��Һ�������Һ����Ѫ��ɫ��˵����Һ����û��Ӧ��FeCl3��Һ��˵���˷�ӦΪ���淴Ӧ������һ�����ȣ�
�ʴ�Ϊ���ݣ���Һ��Ѫ��ɫ��
III������ΪN2O4��g��?2NO2Ϊ���淴Ӧ����Ӧ��ƽ��ʱ����Ӧ���������ʣ���������NO2��N2O4��ƽ��ʱ��n��NO2��=0.12mol/L��0.1L=0.012mol����N2O4�����ʵ���Ϊ0.01mol-0.006mol=0.004mol��
�ʴ�Ϊ��NO2��N2O4��0.004mol��
��v��NO2��=$\frac{��c}{��t}$=$\frac{0.11mol/L-0}{1.1s}$=0.1mol/��L��s����
�ʴ�Ϊ��0.1mol/��L��s����
���� ���⿼��̽����ѧ��Ӧ����Ӱ�����ء���ѧ��Ӧ���ʼ��㡢���淴Ӧ�жϵ�֪ʶ�㣬���ؿ���ѧ��ʵ�������ʵ�����������������̽����������Ի�ѧ��Ӧ����Ӱ��ʱ����ֻ��һ�����ز�ͬ���������ó���ȷ���ۣ���Ŀ�ѶȲ���


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д� �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 3��2 | C�� | 2��3 | D�� | 2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
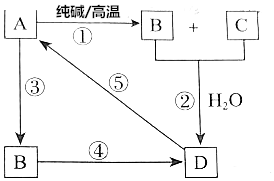 ��֪A��һ�ֲ�����ˮ��������������ͼ��ʾת����ϵ����������пհף�
��֪A��һ�ֲ�����ˮ��������������ͼ��ʾת����ϵ����������пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
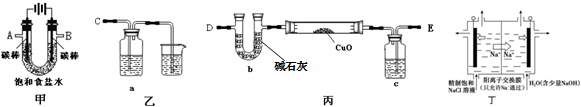
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ӵ��� | B�� | �����¶� | C�� | ��Сѹǿ | D�� | ����O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | A��Һ | B��Һ |
| �� | 2mL 0.2mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ |
| �� | 2mL 0.1mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ |
| �� | 2mL 0.2mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ������MnSO4 |
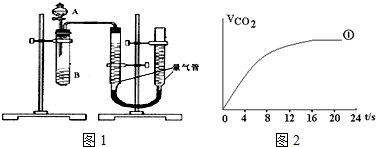
| ʵ���� | 1 | 2 | 3 | 4 |
| ˮ/mL | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/mL | 5 | 5 | 10 | 10 |
| ʱ��/s | 40 | 20 | 10 | --- |
| ʱ��/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| �¶�/�� | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ������Ҫ��Ӧ���Ȼ�ѧ����ʽ��S��s��+O2��g���TSO2��g����H=-297kJ•mol-1 | |
| B�� | ������Ҫ��Ӧ�Ļ�ѧ����ʽ��2SO2+O2$?_{��}^{����}$2SO3 | |
| C�� | ����ʹ�ô��������ѧ��Ӧ���ʺ�ƽ��ת���� | |
| D�� | ��������a ����ֱ���ŷŵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
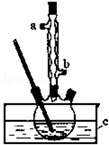 �����ѣ�CH3CH2CH2CH2OCH2CH2CH2CH3����һ�ֻ���ԭ�ϣ�������Ϊ��ɫҺ�壬������ˮ���е�Ϊ142.4�棬�ܶȱ�ˮС��ijʵ��С����������װ�úϳ������ѣ�����װ�þ���ȥ������������Ҫ��ӦΪ��2C3CH2CH2CH2OH$��_{135��}^{ŨH_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
�����ѣ�CH3CH2CH2CH2OCH2CH2CH2CH3����һ�ֻ���ԭ�ϣ�������Ϊ��ɫҺ�壬������ˮ���е�Ϊ142.4�棬�ܶȱ�ˮС��ijʵ��С����������װ�úϳ������ѣ�����װ�þ���ȥ������������Ҫ��ӦΪ��2C3CH2CH2CH2OH$��_{135��}^{ŨH_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C5H12 | C7H16 | C8H16 |
| A�� | 13 | B�� | 14 | C�� | 10 | D�� | 9 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com