
下列说法摘自某些刊物,你认为无科学性错误的是
A.铅笔芯的原料是铅,儿童用嘴咬铅笔会导致铅中毒
B.CO有毒,生有煤炉的居室,可以放数盆水,使生成的CO被吸收,防止中毒
C.硅的提纯与应用,促进了半导体元件与集成芯片的发展,可以说“硅是信息技术革命的催化剂”
D.在农业温室大棚内燃烧煤,产生的CO2不利于植物的生长
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届重庆市高三5月模拟考试理综化学试卷(解析版) 题型:简答题
合成氨工业上常用下列方法制备H2:
方法①:C(s)+2H2O(g) CO2(g)+2H2(g)
CO2(g)+2H2(g)
方法②:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
(1)已知①C(石墨)+O2(g)═CO2(g)△H=-394kJ•mol-1
②2C(石墨)+O2(g)═2CO2(g)△H=-222kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1
试计算25℃时由方法②制备1000gH2所放出的能量为______kJ。
(2)在一定的条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:C(s)+2H2O(g) CO2(g)+2H2(g)其相关数据如下表所示:
CO2(g)+2H2(g)其相关数据如下表所示:
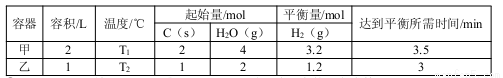
①T1______T2(填“>”、“=”或“<”);T1℃时,该反应的平衡常数K=______。
②乙容器中,当反应进行到1.5min时,H2O(g)的物质的量浓度范围是______。
③在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是______。
A.V逆(CO2)=2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均摩尔质量保持不变
④某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
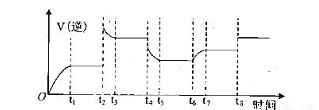
在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是________________________,从t1到t8哪个时间段H2O(g)的平衡转化率最低______。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
关于化学反应与能量的说法正确的是( )
A.中和反应是吸热反应
B.化学键断裂放出能量
C.反应物总能量与生成物总能量一定相等
D.燃烧属于放热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.相同数目的H318O+和D2O分子中的中子数相等
B.5424Cr为铬的一种核素,其核外电子数为30
C.标准状况下,22.4L氦气与22.4L氟气所含原子数均为1.204×1024
D.Na2O2与H2O反应生成氧气,反应中水作还原剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
下列关于SO2性质的说法中,不正确的是
A.能与NaOH溶液反应 B.能使品红溶液褪色
C.能与水反应直接生成硫酸 D.能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
生活中下列处理方法正确的是
A.氯气易液化,液氯可以保存在钢瓶中
B.食盐可作调味剂,不能作食品防腐剂
C.纺织品上的油腻用烧碱溶液清洗
D.把铁器具浸入水隔绝空气防生锈
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
某高分子化合物R的结构简式为右图,下列有关R的说法正确的是
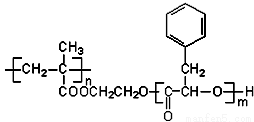
A.R的单体之一的分子式为C9H10O2
B.R完全水解后生成物均为小分子有机物
C.通过加聚反应和缩聚反应可以生成R
D.碱性条件下,1 mol R完全水解消耗NaOH的物质的量为2 mol
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三5月四模化学试卷(解析版) 题型:填空题
甲酸钙广泛用于食品、工、石油等工业生产上,300~400℃左右分解.
Ⅰ、实验室制取的方法之一是:Ca(OH)2+2HCHO+H2O2=Ca(HCOO)2+2H2O+H2↑.
实验室制取时,将工业用氢氧化钙和甲醛依次加入到质量分数为30-70%的过氧化氢溶液中(投料物质的量之比依次为1:2:1.2),最终可得到质量分数98%以上且重金属含量极低的优质产品.
(1)过氧化氢比理论用量稍多,其目的是____________。
(2)反应温度最好控制在30-70℃之间,温度不易过高,其主要原因是____________。
(3)制备时在混合溶液中要加入微量硼酸钠抑制甲醛发生副反应外,还要加入少量的Na2S溶液,加硫化钠的目的是____________。
(4)实验时需强力搅拌45min,其目的是____________;结束后需调节溶液的pH 7~8,其目的是____________,最后经结晶分离、干燥得产品.
Ⅱ、某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合右图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)。
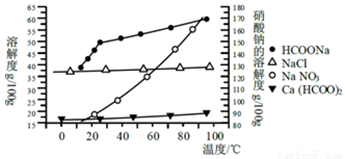
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
请补充完整由碳酸钙制备甲酸钙的实验方案:称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用;____________。
提供的试剂有:a.甲酸钠,B.5mol•L-1硝酸,C.5mol•L-1盐酸,D.5mol•L-1硫酸,e.3%H2O2溶液,f.澄清石灰水。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省黄冈市高三5月一模理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.常温下1L 0.1 mol﹒L-1的FeSO4溶液中含有0.4NA个氧原子
B.用碱性锌锰干电池作电源电解饱和食盐水,当消耗MnO2 8.7g时,可制得标况下氯气2.24L
C.1.2g CaCO3与Mg3N2的混合物中含有质子数为0.6NA
D.常温下,pH=7的0.5 mol/L的CH3COONH4溶液中,NH4+浓度为0.5 mol﹒L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com