
| A�� | ��������FeCl2 | B�� | ����ʹKMnO4��ɫ����NO2- | ||
| C�� | G��pH��7 | D�� | ������Ba��OH��2?AlCl3?Na2SO3��� |
���� �û���������ˮ��ֽ��裬�õ���ɫ����E����ɫ��ҺG����һ������FeCl2������Ϊ���������������ᱵ�����ᱵ��
��ȡ����E����ϡ��������������ɫ���������ܽ⣬����һ����������������ԭ�������һ����AlCl3���������ᱵ��������ԭ�������һ����Na2SO3��
��ȡ����G��μ���ϡ�������������������ɰ�ɫ��������������ܽ⣬����������ᱵ�������ᱵ��G�к������ӣ�ԭ�������һ����Ba��OH��2��
��ȡ����G�μ��������Ը�����أ������յ���ɫ��Һ��һ����NaNO2���Դ������
��� �⣺�û���������ˮ��ֽ��裬�õ���ɫ����A����ɫ��ҺB����һ������FeCl2������Ϊ���������������ᱵ�����ᱵ��
��ȡ����E����ϡ��������������ɫ���������ܽ⣬����һ����������������ԭ�������һ����AlCl3���������ᱵ��������ԭ�������һ����Na2SO3��
��ȡ����G��μ���ϡ�������������������ɰ�ɫ��������������ܽ⣬����������ᱵ�������ᱵ��G�к������ӣ�ԭ�������һ����Ba��OH��2��
��ȡ����G�μ��������Ը�����أ������յ���ɫ��Һ��һ����NaNO2��
A��������������һ��������ɫ�����ӣ���һ������FeCl2����A��ȷ��
B������������������ʹKMnO4��ɫ����NO2-����B��ȷ��
C��G�к�ƫ���ᱵ��ˮ���Լ��ԣ�pH��7����C��ȷ��
D��������NaNO2��Ba��OH��2��AlCl3��Na2SO3��ɣ���D����
��ѡD��
���� ���⿼�����ʵļ��鼰�ƶϣ�Ϊ��Ƶ���㣬���շ����Ļ�ѧ��Ӧ����������۵Ĺ�ϵΪ���Ĺؼ������������ƶ��������ۺ�Ӧ��֪ʶ�����Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ���� | ���ӷ���ʽ |
| �����ʯ��ˮ��ͨ������CO2���� | ||
| ��������Һ��Ͷ������Mg�� | ||
| �������Һ�еμ�NaOH��Һ | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
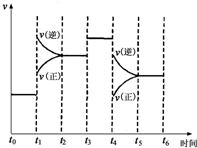 ��ͼ��ʾ��ӦN2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol����ij��ʱ��t0��t6�з�Ӧ�����뷴Ӧ���̵�����ͼ
��ͼ��ʾ��ӦN2��g��+3H2��g��?2NH3��g����H=-92.2kJ/mol����ij��ʱ��t0��t6�з�Ӧ�����뷴Ӧ���̵�����ͼ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ������Һ�У�K+��Mg2+��Cl-��SO42- | |
| B�� | ���д���H+����Һ�У�Na+��Fe2+��NO3-��SO42- | |
| C�� | ij��ɫ��Һ�У�Na+��Al3+��Cl-��HCO3- | |
| D�� | �����£���ˮ�������c��H+��=1��10-12mol•L-1����ɫ��Һ�У�K+��Na+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼΪʵ����ijŨ�����Լ�ƿ��ǩ�ϵ����ݣ�������й����ݻش��������⣺
��ͼΪʵ����ijŨ�����Լ�ƿ��ǩ�ϵ����ݣ�������й����ݻش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{b-2c}{a}$ mol/L | B�� | $\frac{2b-4c}{a}$mol/L | C�� | $\frac{4c-2b}{a}$ mol/L | D�� | $\frac{b-4c}{a}$mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
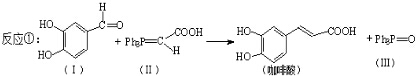
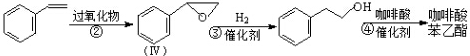
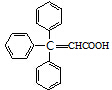 �������ᱽ�����ļ���ʽ�ṹ��ʽΪ
�������ᱽ�����ļ���ʽ�ṹ��ʽΪ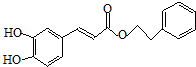 ��
��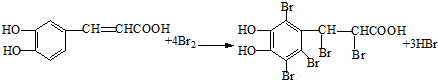 ��
��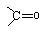
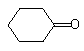 �ķ��㻯���ﹲ��3��
�ķ��㻯���ﹲ��3��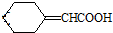 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
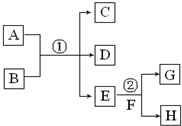 �����и��仯�У�EΪ��ɫ��ζ��Һ�壨�����£���FΪ����ɫ��ĩ��GΪ��������ɫ���壨��Ӧ��������ʡ�ԣ����ش��������⣺
�����и��仯�У�EΪ��ɫ��ζ��Һ�壨�����£���FΪ����ɫ��ĩ��GΪ��������ɫ���壨��Ӧ��������ʡ�ԣ����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com