
(13分)对含氮物质的研究和利用有着极为重要的意义。
(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下:
N2(g)+O2(g)=2NO(g) 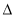 H= +180.5kJ·mol-1;
H= +180.5kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) 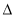 H = -483.6 kJ·mol-1;
H = -483.6 kJ·mol-1;
N2(g)+3H2(g)=2NH3(g) 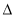 H = -92.4 kJ·mol-1。
H = -92.4 kJ·mol-1。
则氨的催化氧化反应的热化学方程式为 。
(2)汽车尾气净化的一个反应原理为:
2NO(g)+2CO(g) N2(g)+2CO2(g)
N2(g)+2CO2(g) 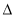 H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如图所示。
H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如图所示。

①NO的平衡转化率为 ,0~20min平均反应速率v(NO)为 。25min时,若保持反应温度不变,再向容器中充入CO、N2各0.8 mol,则化学平衡将 移动(填“向左”、“向右”或“不”)。
②若只改变某一反应条件X,反应由原平衡I达到新平衡II,变量Y的变化趋势如下图所示。下列说法正确的是 (填字母代号)。

(3)某化学小组拟设计以N2和H2为电极反应物,以HCl—NH4Cl为电解质溶液制成燃料电池,则该电池的正极反应式为 。假设电解质溶液的体积不变,下列说法正确的是 (填字母代号)。
a.放电过程中,电解质溶液的pH保持不变
b.溶液中的NH4Cl浓度增大,但Cl-离子浓度不变
c.每转移6.02×1023个电子,则有标准状况下11.2L电极反应物被氧化
d.为保持放电效果,电池使用一段时间需更换电解质溶液
(13分)
(1)4NH3(g)+5O2(g)====4NO(g) +6H2O(g) ΔH=﹣905kJ·mol-1(2分)
(2)① 28.6%(2分) 0.02 mol·L-1·min-1(2分) 向左(1分)
② b(2分)
(3) N2+8H++6e-=2NH4+ (2分) ,bcd(2分,少选一个得1分,多选、错选不得分)
【解析】
试题分析:(1)将已知热化学方程式中的氮气、氢气按照盖斯定律消去,可得氨气的催化氧化的热化学方程式为:4NH3(g)+5O2(g)====4NO(g) +6H2O(g) ΔH=﹣905kJ·mol-1;
(2)①根据图像可知生成氮气的物质的量是0.4mol,则消耗NO的物质的量是0.8mol,所以NO的转化率是0.8mol/2.8mol 100%=28.6%;20min时反应达到平衡,则NO的反应速率是0.8mol/2L/20min=0.02 mol·L-1·min-1; 根据图像可计算NO的浓度是1.0mol/L,CO的浓度是0.8mol/L,氮气的浓度是0.2mol/L,二氧化碳的浓度是0.4mol/L,所以平衡常数K=0.42×0.2/0.8×1=0.04,若保持反应温度不变,再向容器中充入CO、N2各0.8 mol,则此时CO的浓度是1.2mol/L,氮气的浓度是0.6mol/L,浓度商是0.42×0.6/1×1.2=0.08>0.04,所以平衡向左移动;
100%=28.6%;20min时反应达到平衡,则NO的反应速率是0.8mol/2L/20min=0.02 mol·L-1·min-1; 根据图像可计算NO的浓度是1.0mol/L,CO的浓度是0.8mol/L,氮气的浓度是0.2mol/L,二氧化碳的浓度是0.4mol/L,所以平衡常数K=0.42×0.2/0.8×1=0.04,若保持反应温度不变,再向容器中充入CO、N2各0.8 mol,则此时CO的浓度是1.2mol/L,氮气的浓度是0.6mol/L,浓度商是0.42×0.6/1×1.2=0.08>0.04,所以平衡向左移动;
②a.压强增大,平衡常数不变,错误;b.温度升高,平衡逆向移动,则CO的平衡浓度增大,符合图像,正确;c.温度升高,平衡逆向移动,氮气的体积分数降低,与图不符,错误;d.使用催化剂,对平衡无影响,所以NO的转化率不变,错误,答案选b;
(3)以N2和H2为电极反应物,以HCl—NH4Cl为电解质溶液制成燃料电池,则氮气发生还原反应,氢气发生氧化反应,所以正极是氮气得到电子,与氢离子结合生成铵根离子,电极反应式为N2+8H++6e-=2NH4+;负极的反应式为H2-2e-=2H+,所以总反应方程式为N2+2H++ 3H2=2NH4+;则放电过程中,氢离子浓度降低,pH增大,a错误;因为该过程中生成铵根离子,所以溶液中的NH4Cl浓度增大,但Cl-的物质的量不变,所以氯离子离子浓度不变,b正确;每转移6.02 1023个电子,即1mol电子,则有0.5mol氢气被氧化, 标准状况下的体积是11.2L,c正确;随着反应的进行,氯化铵的浓度增大,而HCl的浓度逐渐减小,所以为保持放电效果,电池使用一段时间需更换电解质溶液,d正确,答案选bcd。
1023个电子,即1mol电子,则有0.5mol氢气被氧化, 标准状况下的体积是11.2L,c正确;随着反应的进行,氯化铵的浓度增大,而HCl的浓度逐渐减小,所以为保持放电效果,电池使用一段时间需更换电解质溶液,d正确,答案选bcd。
考点:考查对原电池反应原理的应用、盖斯定律的应用,化学平衡移动的判断


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2014-2015学年福建省宁德市五校高二上学期期中化学试卷(解析版) 题型:选择题
下列关于电化学知识说法正确的是
A.电解AlCl3溶液,在阴极上析出金属Al
B.氢氧燃料电池中,氧气是正极反应物
C.用惰性电极电解CuSO4溶液一段时间,溶液酸性不变
D.铅蓄电池在充电时,连接电源正极的电极反应为:PbSO4+2e-=== Pb+SO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省焦作市高三上学期期中化学试卷(解析版) 题型:选择题
下列各反应对应的离子方程式正确的是
A.向100 mL 0.12 mol/L的Ba(OH)2溶液中通入0.02 mol CO2:OH-+CO2 = HCO3-
B.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2+ + 2OH-+2HCO3- = CaCO3↓+ CO32-+ 2H2O
C.向0.2 mol溴化亚铁溶液中通入0.2 mol氯气:2Fe2++4Br-+3Cl2 = 2Fe3++6Cl-+2Br2
D.硫酸氢钠与氢氧化钡两种溶液反应后pH恰好为7:H++SO42-+Ba2++OH-= BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三上学期期中理综化学试卷(解析版) 题型:选择题
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y: 154pm Z:125pm W: 117pm,X Y W位置如图所示(副族省略),
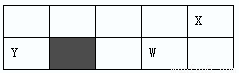
X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是
A.元素Z处于周期表的阴影位置
B.非金属性:X>W
C.X与W形成化合物熔点很高,为离子化合物
D.Y、W的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三上学期期中理综化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.淀粉是天然高分子化合物
B.甲醛广泛应用于食品加工
C.溴乙烷和甲醇都能发生消去反应
D.聚丙烯能使溴水褪色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省等四校高三上学期期中联考化学试卷(解析版) 题型:选择题
叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵中全都是共价键
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-) >c(OH-)>c(H+)
D.N3-与CO2含相等电子数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省等四校高三上学期期中联考化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入到FeC12溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca (OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2
A.①②③④⑤ B.只有①④ C.只有②③ D.只有③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是
A.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
B.W与X形成的化合物中只含离子键
C.X、Y、Z、W的原子半径依次减小
D.若W与Y原子序数相差5,则二者形成化合物的化学式一定为Y2W3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省高三上学期第二次模考试化学试卷(解析版) 题型:选择题
在密闭容器中,加热等物质的量的NaHCO3和Na2O2的固体混合物,充分反应后,容器中的固体剩余物是
A.Na2CO3和Na2O2 B.Na2CO3和NaOH
C.NaOH和Na2O2 D.NaOH、Na2O2和Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com