
| A、21:5 | B、11:3 |
| C、3:1 | D、4:1 |


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
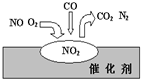 在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示.下列说法错误的是( )
在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示.下列说法错误的是( )| A、NO2是红棕色气体 | ||||
| B、NO和O2必须在催化剂表面才能反应 | ||||
| C、汽车尾气的主要污染成分包括CO和NO | ||||
D、催化转化总反应为:2NO+O2+4CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、YM2晶体中Y原子为sp3杂化 |
| B、由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| C、Z、M形成的两种分子都是极性分子 |
| D、WM3-的空间构型为平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的原子半径:A<B<C<D<E |
| B、对应氢化物的热稳定性:D>E |
| C、B与C、B与D形成的化合物中化学键类型相同 |
| D、五种元素中最高价氧化物对应的水化物酸性最强的是E. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验次数 | 样品质量/g | 沉淀质量/g |
| 1 | 1.716 | 2.758 |
| 2 | 2.574 | |
| 3 | 3.432 | 5.516 |
| 4 | 4.290 | 5.516 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2w1=w2 |
| B、2w2=w1 |
| C、w2>2w1 |
| D、w1<w2<2w1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com