
|
元素X原子的核内中子数与核外电子数相等.将2.8 g X的单质在过量的氧气中充分燃烧,得6.0 g氧化物XO2.X在元素周期表中的位置是 | |
A. |
第2周期 |
B. |
第3周期 |
C. |
ⅣA族 |
D. |
ⅤA族 |
|
由题意可知:X与O2发生化学反应X+O2 参加反应的O2的质量是6.0 g-2.8 g=3.2 g,也是0.10 mol. 综合上述可知,2.8 g X的物质的量是0.10 mol.则元素X的摩尔质量是28 g/mol,相对原子质量是28. 题中还有一项已知的条件是元素X原子的核内中子数与核外电子数相等,题目又要求判断X在元素周期表中的位置. 在任意的中性原子中都具有微粒关系:质量数=质子数+中子数,质子数=电子数 在X的原子中还具有特殊的微粒关系:中子数=电子数=质子数 则元素X的原子核内质子数为28÷2=14 质子数为14的原子,原子结构示意图为. 原子的电子层数是3,元素位于周期表的第3周期;最外层电子数是4,元素位于周期表的ⅣA族. |
|
该题的命题创新在于将质量守恒和化学计算容于根据原子结构判断元素在周期表中的位置.命题创新必然要解题创新. |


科目:高中化学 来源:物理教研室 题型:021
(A)第三周期 (B)第二周期 (C)第Ⅳ主族 (D)第Ⅴ主族
查看答案和解析>>
科目:高中化学 来源: 题型:021
某元素x原子的核外电子数等于核内中子数,取2.8g该元素的单质与氧充分作用,可得到6g化合物XO2。该元素在周期表中的位置是 ( )
(A)第三周期 (B)第二周期
(C)第Ⅳ主族 (D)第Ⅴ主族
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
某元素X的气态氢化物表示为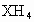 ,其中X的质量分数为75%,X原子的核内有6个中子,核电荷数是____________,最外层电子数是__________,该元素位于周期表中第_______周期_________族,元素名称_________,其最高价氧化物化学式是__________.
,其中X的质量分数为75%,X原子的核内有6个中子,核电荷数是____________,最外层电子数是__________,该元素位于周期表中第_______周期_________族,元素名称_________,其最高价氧化物化学式是__________.
查看答案和解析>>
科目:高中化学 来源:北京期中题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com