
| A. | 生活中,用冰箱保存食物 | |
| B. | H2O2分解时,用MnO2 作催化剂 | |
| C. | 工业合成氨时,采用高温高压的措施 | |
| D. | 提高反应物的浓度 |
科目:高中化学 来源: 题型:选择题
| A. | 熟石膏的化学式:2CaSO4•H2O | B. | 明矾的化学式KAlSO4•12H2O | ||
| C. | CaCl2的电子式: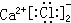 | D. | 氯化钠的电子式Na:$\underset{\stackrel{..}{Cl}}{..}$: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3(AgNO3) | B. | NaOH(NaOH) | C. | KCl(KCl) | D. | CuSO4(CuO) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
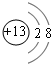 .
.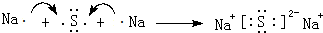 .
.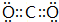 ,该分子的结构式为O=C=O.
,该分子的结构式为O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 防止电池中汞、镉和铅等重金属离子污染土壤和水源 | |
| B. | 回收利用石墨电极和金属材料 | |
| C. | 充电后可再使用 | |
| D. | 防止电池中的电解质溶液腐蚀其他物品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 以H2为燃料的新型燃料电池,电池的工作示意图所示.若此电池以KOH为电解质溶液,试回答下列问题:
以H2为燃料的新型燃料电池,电池的工作示意图所示.若此电池以KOH为电解质溶液,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.336L | B. | 0.448L | C. | 0.896 L | D. | 1.344L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com