
已知常温下硫酸钡的溶度积Ksp=10-10,求该温度下硫酸钡的溶解度(原子量:Ba:137 S: 32 O:16)___________________。
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
(Ⅰ)(9分)
现有下列物质: ①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)在上述状态下能导电的物质是 ;
(2)属于弱电解质的是 ;
(3)属于非电解质,但溶于水后的水溶液能导电的是 ;
(Ⅱ)现有下列电解质溶液:①![]() ②
②![]() ?③
?③![]() ? ④
? ④![]() ⑤
⑤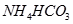 (已知酸性
(已知酸性![]() 。)
。)
(1)在这五种电解质溶液中,既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)常温下,物质的量浓度相同的①、②、③溶液pH大小顺序为(填序号) > > 。
(3)写出⑤与足量NaOH溶液混合加热时反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷 题型:填空题
(Ⅰ)(9分)
现有下列物质: ①NaCl晶体 ②液态SO2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KCl ⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)在上述状态下能导电的物质是 ;
(2)属于弱电解质的是 ;
(3)属于非电解质,但溶于水后的水溶液能导电的是 ;
(Ⅱ)现有下列电解质溶液:①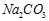 ②
②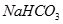 ?③
?③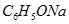 ? ④
? ④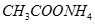 ⑤
⑤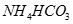 (已知酸性
(已知酸性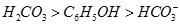 。)
。)
(1)在这五种电解质溶液中,既能与盐酸又能与烧碱溶液反应的是(填写序号) 。
(2)常温下,物质的量浓度相同的①、②、③溶液pH大小顺序为(填序号) > > 。
(3)写出⑤与足量NaOH溶液混合加热时反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2010届靖江高级中学高三第三次模拟考试化学试题 题型:实验题
(10分) 二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂,常温下二氧化氯为黄绿色或橘黄色气体,易溶于水,易与碱液反应,其性质非常不稳定,温度过高、二氧化氯的水溶液质量分数高于30%等均有可能引起爆炸。某研究小组设计下图所示实验装置制备ClO2。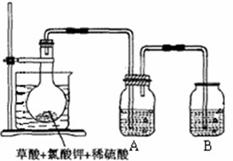
现称取12.25gKClO3和9g草酸(H2C2O4)放入烧瓶中,然后再加入足量的稀硫酸,水浴加热。
回答下列问题:
(1)已知反应后的产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为 。
(2)在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其保持在60℃~
80℃之间。这样操作的目的是 ,
图示装置中缺少的一种必须的玻璃仪器是 。
(3)A装置用于吸收产生的二氧化氯,其中最好盛放 (填序号)。
a. 50mL 60℃的温水 b. 50mL冰水 c. 50mL饱和食盐水 d. 50mL NaOH溶液
(4)本实验所制得的二氧化氯水溶液质量分数约为 。(小数点后保留两位)
(5)二氧化氯可迅速氧化硫化物,以除去有机硫产生的臭味,改善水产养殖水体的水质。取适量二氧化氯溶液加入到硫化氢溶液中,再向其中加入少量氯化钡溶液,发现有白色沉淀生成。硫化氢溶液与二氧化氯发生反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
①5种元素的原子半径按A、B、C、D、E的顺序从大到小排列;
②B、C均是地壳中含量较高的元素,B元素单质常温下遇浓硫酸钝化,C元素的单质及其氧化物的晶体结构成空间网状;
③C、D元素原子最外层电子数之和与A、B元素原子最外层电子数之和相同,而且E元素原子的最外层电子数为A、B、C、D四种元素原子最外层电子数之和的四分之一;
④E元素的一种氧化物能与水反应生成该元素最高价氧化物的水化物,同时生成E的另一种氧化物。
请回答以下问题:
(1)C元素原子结构示意图为___________;E的气态氢化物的电子式为___________;
(2)写出B的最高价氧化物的水化物在水中的电离方程式___________;
(3)D的某种氧化物中D元素的质量分数是50%,则该氧化物的性质有(填字母)___________;
A.可使溴水褪色 B.可使品红溶液褪色
C.通入氯化钡溶液,产生白色沉淀 D.溶于水,生成强酸
(4)A单质的浓溶液与一种有机物(C8H6O)反应能生成白色沉淀,写出有关反应的化学方程式___________________________________________ _________________________;
(5)E元素的气态氢化物可与热的氧化铜反应得到E的单质,每0.1 mol氧化铜完全反应时转移0.2 mol电子,写出有关反应的化学方程式________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com