
����Ŀ����֪A��B��C��D��E��F��G�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����������������A��B��C��D��EΪ��ͬ�����Ԫ�ء�A��C��������������������Ӳ�����2����B�ĵ縺�Դ���C������ɫ�ܲ����۲�E����ɫ��ӦΪ��ɫ��F�Ļ�̬ԭ������4��δ�ɶԵ��ӣ�G��+1�����������ó���K��L��M�������Ӳ㡣�ش��������⣺
��1��A��B��C��D��E��F��G����Ԫ���е�һ��������С��������Ԫ�ط�������DԪ�ص�ԭ�Ӻ������ֲ�ͬ�˶�״̬�ĵ��ӣ����ֲ�ͬ�ܼ��ĵ��ӡ���̬��F3+��������Ų�ʽ�ǡ�
��2��B����̬�⻯����ˮ�е��ܽ��Զ����A��C����̬�⻯�ԭ���ǡ�
��3��������ECAB�е���������AC2��Ϊ�ȵ����壬�������ӵĵ���ʽ�ǡ�
��4��FD3��ECAB��Һ��ϣ��õ�������������Ѫ��ɫ��Һ��������λ��Ϊ5�������Ļ�ѧʽ�ǡ�
��5��������EF[F��AB��6]��һ����ɫ���壬��ͼ��ʾ�侧����1/8��E+δ������������ɫ�����һ��������E+�ĸ���Ϊ��
��6��G�Ķ��������������Ҷ�����H2N��CH2һCH2��NH2���γ������ӣ�
![]()

���������к��еĻ�ѧ�������С�������ĸ��
a�����
B�����Լ�
C�����Ӽ�
D���Ǽ��Լ�
������CAB-�е�Aԭ�����Ҷ�����H2N��CH2һCH2��NH2����Cԭ�ӵ��ӻ���ʽΪ��
���𰸡���1��K1751s22s22p63s23p63d5
��2��NH3��H2O���Ӽ���������CH4��H2S������H2O���Ӽ䲻�������
��3��[![]() ]-
]-
��4��K2Fe��SCN��5
��5��4��6��abdspsp3
��������
���������A��B��C��D��E��F��G�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵������������A��B��C��D��EΪ��ͬ�����Ԫ�أ�A��C��������������������Ӳ�����2����AΪC��CΪSԪ�أ�����ɫ�ܲ����۲�E����ɫ��ӦΪ��ɫ����EΪKԪ�أ�Dԭ����������C��С��EΪ����Ԫ�أ���D��ClԪ�أ�B�ĵ縺�Դ���C����ԭ������С��C��������Ԫ�ش��ڲ�ͬ���壬��BΪNԪ�أ�F�Ļ�̬ԭ������4��δ�ɶԵ��ӣ���λ�ڵ�������Ԫ�أ���FΪFeԪ�أ�G��+1�����������ó���K��L��M�������Ӳ㣬��GΪCuԪ�أ�
��1��Ԫ�صĽ�����Խǿ�����һ������ԽС���⼸��Ԫ���н�������ǿ����K�����һ��������С����K��D��ClԪ�أ�ԭ�Ӻ�����17�����ӣ����Ӿ���17���˶�״̬����5�ֲ�ͬ���ܼ���F��FeԪ�أ�ʧȥ�����������������ӣ������Ӻ�����23�����ӣ����ݹ���ԭ��֪�����Ӻ�������Ų�ʽΪ1s22s22p63s23p63d5��
��2��B���⻯���ǰ�����C���⻯�������⡢A���⻯���Ǽ��飬���⡢�����ˮ���Ӳ����γ������������ˮ�������γ����������Ĵ��ڴٽ����ܽ���������������ܽ�ȴ��ڼ�������⣻
��3��SCN���ĵ���ʽΪ��[![]() ]����
]����
��4��FeCl3��KSCN��Һ��ϵõ�������������Ѫ��ɫ��Һ�����ɵ������Ϊ���軯�أ�������λ��Ϊ5�������Ļ�ѧʽ��K2Fe��SCN��5��
��5����ͼ1��E+δ���������þ�����Fe2+����=8��4��1/8=4��Fe3+����=8��4��1/8=4��CN-����=12����8=24�����ݻ������и�Ԫ�ػ��ϼ۵Ĵ�����Ϊ0֪��K+����=��24��1-4��2-4��3��/1=4��
��6��Cu�Ķ��������������Ҷ�����H2N-CH2һCH2һNH2���γ�����������ͼ����C-Cԭ��֮����ڷǼ��Լ���C-N��C-H��N-Hԭ��֮����ڼ��Լ���ͭ���Ӻ͵�ԭ��֮�������λ�������Ը��������к��еĻ�ѧ����������λ�������Լ����Ǽ��Լ�����ѡabd��SCN�����е�Cԭ�۲���ӶԸ�����2�Ҳ����µ��Ӷԣ�����Cԭ���ӻ���ʽΪsp���Ҷ�����H2N-CH2һCH2һNH2����Cԭ�Ӽ۲���ӶԸ�����4�Ҳ����µ��Ӷԣ�����C���ӻ���ʽΪsp3��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij���ݻ�Ϊ2 L���ܱ������ڣ���T��ʱ����ͼ1��ʾ������Ӧ��

mA(g)+nB(g)![]() pD(g)+qE(s) H<0��m��n��p��q����������������
pD(g)+qE(s) H<0��m��n��p��q����������������
��1������ͼ1��ʾ����Ӧ��ʼ���ﵽƽ��ʱ����D��ʾ�÷�Ӧ����Ϊ____________ mol/��L��min��������ʽ��m:n:p:q =________________
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ��KΪ_________________(������һλС��)��
��3�����д�ʩ������B��ת���ʵ��� �� ��
A�������¶� B�������������ͨ��1molB
C��������������Ƴ���������D(g) D�����������ݻ�����Ϊԭ����2��
E. �����������ͨ��1mol A
��4�����жϸ÷�Ӧ�Ѿ��ﵽ��ѧƽ��״̬���ǣ� ��
A�����ݺ���ʱ����������ѹǿ���ֲ���
B�����������DŨ�Ȳ���
C��v(A)�� = v(A)��
D������ʱ�����������ܶȲ���
��5����Ӧ�ﵽƽ���7 minʱ���ı��������ڵ�9min�ﵽ�µ�ƽ�⣬��ͼ2��������7 min����15 min�����ڴ���ֽ�ϣ�����������£�DŨ���仯ͼ��
���������¶���ƽ��ʱD���ʵ����仯��0.4 mol (������)
�������������ݻ�ѹ��Ϊԭ��һ��(��ʵ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������A��B��C��D��E����ԭ��������������Ķ�����Ԫ�أ����������еĶ�����Ԫ���У�A��ԭ�Ӱ뾶��D��ԭ�Ӱ뾶֮����С��������ϡ�����壩��C��A��B��D�����γɶ��ֳ��������BԪ�ص�����������Ӧ��ˮ���������⻯�ﷴӦ����һ���Σ�������AE������Ϊ���塣�ش��������⣺
��1��A�ֱ���B��C�γɵ���������У��ȶ��� �� ���÷���ʽ��ʾ��������A��B�γɵ����������ӵĿռ乹��Ϊ ��
��2��������ס��Ҿ�������������Ԫ���е�������ɵ�ǿ����ʣ��ҳ������������ʵ�ˮ��ҺpH������7�����Ԫ�ص�ԭ����Ŀ�Ⱦ�Ϊ1��1��1����������ij�ּ�������Һ����Ч�ɷ֣�����ĵ���ʽΪ ��
��3�����������C��D����Ԫ����ɣ�����C��D��ԭ�Ӹ�����Ϊ1��1������к��еĻ�ѧ�������� ��
��4��BԪ�ص�����������Ӧ��ˮ���������⻯�ﷴӦ���ɵ��ε�ˮ��Һ�� �ԣ����������������������������������ӷ���ʽ����ԭ�� ��
��5��д��ʵ������ȡ����E�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ���ǣ� ��
A��ϡ�������ͭƬ�ϣ�Cu��2H�� = Cu2����H2��
B����CH3COOH��Һ�м���CaCO3��2 CH3COOH��CaCO3 = 2 CH3COO����Ca2����H2O��CO2��
C��ϡ������Ba(OH)2��Һ��ϣ�H��+ SO![]() ��OH��+ Ba2�� = BaSO4��+H2O
��OH��+ Ba2�� = BaSO4��+H2O
D��NaOH��Һ��KHCO3��Һ�����OH�� + HCO3�� = H2O +CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��A��B��C��D��E��ԭ������������������B��Eͬ���塣AԪ�ص���������ϼۺ�������ϼ۵ľ���ֵ֮��Ϊ2��1 mol C��������ˮ��Ӧ���ڱ�״��������11.2 L H2��Dԭ����������������������������E���ĵ��Ӳ�ṹ��Arԭ����ͬ��
��1����Ԫ�ط��ű�ʾ��Ԫ��A________��B_________��C_________��D__________��E_________��
��2�����γɹ��ۼ���Ԫ��
��3��A�ĵ��ʵĵ���ʽΪ______________
��4��C��B�γɻ�����ĵ���ʽ__________
��5��д��C��ˮ��Ӧ�����ӷ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɢ�����Ӵ�С��__________֮��ķ�ɢϵ���н��塣�Ʊ� Fe(OH)3����������е�����ˮ����μ���_________������Һ�������������Һ��_________�� ͣ ֹ �� �� �� �� �� Fe(OH)3 �� �� �� �� ѧ �� �� ʽ Ϊ: _________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������0.1000 mol/L NaOH��Һ�ֱ�ζ�20.00 mL 0.1000 mol/L HCl��Һ��20.00 mL 0.1000 mol/L CH3COOH��Һ���õ�2���ζ����ߣ�����ͼ��ʾ��

ͼ1 ͼ2
��1��CH3COOH�ĵ��뷽��ʽ�� ��
��2����A��C���жϣ��ζ�HCl��Һ�������� ���ͼ1����ͼ2������ͼ����a = mL��
��3����NaOH��Һ�ζ�CH3COOHʱѡ�� ��ָʾ������V(NaOH)=10.00 mLʱ���ζ�CH3COOH������Һ�е������غ�ʽ�� ��
��4��D����ʾ��Һ��c(Na+) c(CH3COO��)���������������������������
��5��E���Ӧ����ҺpH��7��ԭ���� �������ӷ���ʽ��ʾ������Һ������Ũ���ɴ�С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ѧϰС���ͬѧ��������������ԭ��Ӧ���ԭ��أ�2KMnO4��10FeSO4��8H2SO4==2MnSO4��5Fe2(SO4)3��K2SO4��8H2O������װ�б���K2SO4��Һ��������������ȷ����

A. ���ձ��з�����ԭ��Ӧ
B. ���ձ�����Һ��pH��С
C. ��ع���ʱ�������е�SO42-������ձ�
D. ���·�ĵ��������Ǵ�a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڽӴ���������������У�SO2ת����SO3ת���ʵĴ�Сֱ�Ӿ�������Ч�ʡ�ij�о�С������ͼװ��ģ�����������вⶨSO2ת����SO3��ת���ʡ���֪SO3���۵���16.8�棬�е���44.8�档����װ�������漰��Ӧ�Ļ�ѧ����ʽΪ��
Na2SO3(s)+H2SO4(75%)=Na2SO4+SO2��+H2O
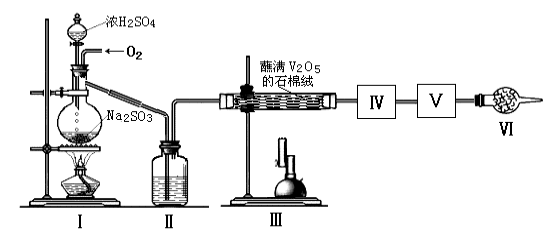
��1�����е��Լ��� ��������������Ϊ ��
��2������ʵ����Ҫ��Ӧ���������������Ӻ��ʵ�װ�á������ͼA��Dװ����ѡ�����ʺ�װ�ò��������������Ŀո��У������������ӵ�װ�÷ֱ��� �� ��
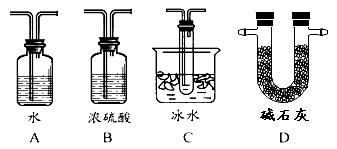
��3��Ϊ�����SO2��ת���ʣ�ʵ��ʱ�ڣ��ٵμ�Ũ�����������ȴ����IJ����У�Ӧ��ȡ�IJ�������_______��_________(����)��
��4��ʵ�������������ռ�SO3���Թ�����¶���ڿ����У��ܹ������ܿ��д����İ����������������ԭ���� ��
��5����18.9gNa2SO3��ĩ��������Ũ��������д�ʵ�飬����Ӧ����ʱ������ͨ��O2һ��ʱ�����װ����������7.2g����ʵ����SO2��ת����Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com