
【题目】(1)已知:①Fe(s)+1/2O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
②2Al(s)+3/2O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是__________________________。某同学认为,铝热反应可用于工业炼铁,你的判断是________(填“能”或“不能”),你的理由是_________________。
(2)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。

①据图判断该反应是________(填“吸”或“放”)热反应
②其中B历程表明此反应采用的条件为_____ (填字母)。
A.升高温度 B.增大反应物的浓度 C.降低温度 D.使用催化剂
科目:高中化学 来源: 题型:
【题目】NO2 与SO2能发生反应:NO2+SO2![]() SO3+NO,某研究小组对此进行相关实验探究。
SO3+NO,某研究小组对此进行相关实验探究。
(1)已知:2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0kJmol-1
2NO2(g) ΔH=-113.0kJmol-1
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJmol-1
2SO3(g) ΔH=-196.6kJmol-1
则NO2(g)+SO2(g)![]() SO3(g)+NO(g) ΔH=______________________。
SO3(g)+NO(g) ΔH=______________________。
(2)实验中,尾气可以用碱溶液吸收。NaOH 溶液吸收NO2时,发生的反应为:2NO2+2OH-=NO2-+NO3-+H2O,反应中的还原剂是__________;用NaOH 溶液吸收少量SO2的离子方程式为______________________________。
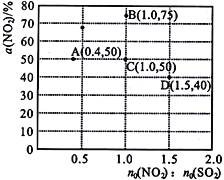
(3)在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2)∶n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如图所示:
①当容器内_____(填标号)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强 b.气体的平均摩尔质量
c.气体的密度 d.NO2的体积分数
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是______________。
③若A 点对应实验中,SO2(g)的起始浓度为c0 molL-1,经过t min达到平衡状态,该时段化学反应速率v(NO2)=______________mol·L-1·min-1。
④图中C、D 两点对应的实验温度分别为Tc和Td,通过计算判断:Tc____Td(填 “>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下 列叙述不正确的是( )

A. 若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛Na2SiO3,则C中溶液中变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 实验仪器D可以起到防止溶液倒吸的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧只生成CO2和H2O,两者的物质的量之比为2∶3,因而可以说
A. 该有机物中含C、H、O三种原子
B. 该化合物是乙烷
C. 该化合物中C、H原子个数比为2:3
D. 该化合物中含C原子和H原子,但不能确定是否含有O原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃组成的混合气体0.1 mol,完全燃烧得0.16 mol CO2和3.6 g H2O,下列说法正确的是
A. 混合气体中一定有甲烷 B. 混合气体一定是甲烷和乙烯
C. 混合气体中可能有乙炔 D. 混合气体中一定有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种元素在周期表中的位置如下图所示,已知A、B、C原子序数之和为37。下列关于A、B、C三种元素的说法正确的是
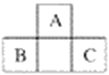
A. 元素B和C位于第四周期 B. 元素A的原子序数为7
C. 元素B最外层有5个电子 D. 元素C位于第三周期ⅤA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O,其中1mol氧化剂在反应中得到的电子为( )
A.10mol
B.11mol
C.12mol
D.13mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.材料的不断发展可以促进社会进步.
(1)钢铁是制造航母的主要材料,钢铁在潮湿空气中易发生________ 腐蚀,其负极反应是________ .请列举一种防止钢铁腐蚀的方法:________ .
(2)不锈钢丝与棉纤维可织成一种防辐射布料.这种布料属于________ (填字母).
a.合金材料 b.复合材料 c.陶瓷材料
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机.请写出高纯硅和氮气在1300℃时反应制备氮化硅的化学方程式:________ .
II.我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
(1)往燃煤中加入________ (填化学式),可大大减少产物中的SO2 .
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是________ (填化学式).治理废水中的重金属污染物可用沉淀法.例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为________ (填化学式)沉淀而除去.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com