
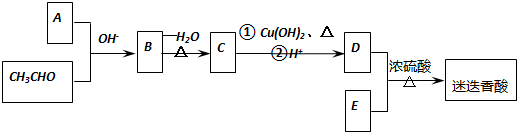
 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$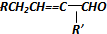
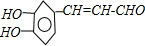 .
. .
. 、
、 、
、 、
、 (任一种).
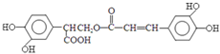
(任一种).分析 D与E在浓硫酸、加热条件下合成迷迭香,由迷迭香酸分子结构 可知,该反应为酯化反应,迷迭香酸在无机酸作用下发生水解生成
可知,该反应为酯化反应,迷迭香酸在无机酸作用下发生水解生成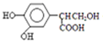 、
、 ;A与CH3CHO反应生成B,再经过系列转化为D,结合迷迭香酸分子酸性水解产物、反应信息①可知,A中含有-CHO,由苯环上取代基及位置可知,A为
;A与CH3CHO反应生成B,再经过系列转化为D,结合迷迭香酸分子酸性水解产物、反应信息①可知,A中含有-CHO,由苯环上取代基及位置可知,A为 ;A与CH3CHO反应生成B
;A与CH3CHO反应生成B ,B失水生成C
,B失水生成C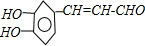 ,C被氢氧化铜氧化生成D,即醛基被氧化成羧基,所以D的结构简式为
,C被氢氧化铜氧化生成D,即醛基被氧化成羧基,所以D的结构简式为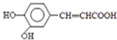 ,故E为
,故E为 .
.
解答 解:A与CH3CHO反应生成B,再经过系列转化为D,结合迷迭香酸分子酸性水解产物、反应信息①可知,A中含有-CHO,由苯环上取代基及位置可知,A为 ;A与CH3CHO反应:
;A与CH3CHO反应: +CH3CHO$\stackrel{OH-}{→}$
+CH3CHO$\stackrel{OH-}{→}$ ,
,
B为: ,B失水生成C
,B失水生成C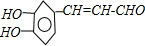 ,C被氢氧化铜氧化生成D,即醛基被氧化成羧基,所以D的结构简式为
,C被氢氧化铜氧化生成D,即醛基被氧化成羧基,所以D的结构简式为 ,故E为
,故E为 ,D与E在浓硫酸、加热条件下发生酯化反应合成迷迭香酸,该反应为:
,D与E在浓硫酸、加热条件下发生酯化反应合成迷迭香酸,该反应为: +
+
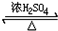
 .
.
(1)通过以上分析知,A为 ,所以A的分子式为C7H6O3,
,所以A的分子式为C7H6O3,
故答案为:C7H6O3;
(2)根据上面的分析可知,C为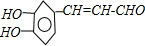 ,
,
故答案为;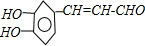 ;
;
(3)通过以上分析知,D为 ,E为
,E为 ,由信息②可知,E中羧基与醇羟基通过酯化反应进行的缩聚反应生成高聚物,其反应方程式为
,由信息②可知,E中羧基与醇羟基通过酯化反应进行的缩聚反应生成高聚物,其反应方程式为 ,
,
故答案为: ;
;
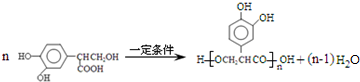
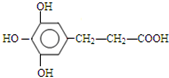
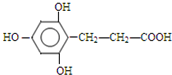
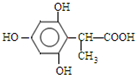
(4) 的同分异构体,苯环上共有四个取代基,且苯环上只有一种化学环境的氢原子,说明苯环上有1种H原子,故四个取代基相同或两组相同的取代基或3个取代基相同、另1个不同,1mol该同分异构体分别与NaHCO3、NaOH反应时,最多消耗NaHCO3、NaOH的物质的量分别是1mol、4mol,说明分子中含有1个-COOH,结合E的结构可知,应还含有3个酚羟基,含有羧基的侧链为-CH2CH2COOH或-CH(CH3)COOH,取代基位置关系为:①三个酚羟基相邻、含有羧基的侧链与3个酚羟基之间的酚羟基处于对位位置,②3个酚羟基处于间位、含有羧基的侧链位于两个酚羟基之间,故符合条件的同分异构体为:
的同分异构体,苯环上共有四个取代基,且苯环上只有一种化学环境的氢原子,说明苯环上有1种H原子,故四个取代基相同或两组相同的取代基或3个取代基相同、另1个不同,1mol该同分异构体分别与NaHCO3、NaOH反应时,最多消耗NaHCO3、NaOH的物质的量分别是1mol、4mol,说明分子中含有1个-COOH,结合E的结构可知,应还含有3个酚羟基,含有羧基的侧链为-CH2CH2COOH或-CH(CH3)COOH,取代基位置关系为:①三个酚羟基相邻、含有羧基的侧链与3个酚羟基之间的酚羟基处于对位位置,②3个酚羟基处于间位、含有羧基的侧链位于两个酚羟基之间,故符合条件的同分异构体为: 、
、 、
、 、
、 ,共4种,
,共4种,
故答案为:4; 、
、 、
、 、
、 (任一种).
(任一种).
点评 本题考查有机物的推断与合成,主要涉及官能团的转化、碳链的变化、官能团性质、同分异构体以及对反应信息的理解利用,充分利用迷迭香酸的分子结构结合反应信息进行判断,理解反应信息是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料 | |
| B. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| C. | 在农村推广使用沼气 | |
| D. | 减少资源消耗、增加资源的重复使用和资源的循环再生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过煤的直接或间接液化可以获得各种芳香烃 | |
| B. | 通过石油的催化重整等工艺可获取芳香烃 | |
| C. | 石油的裂化的目的主要是为了提高轻质油的产量 | |
| D. | 石油的裂解的目的主要是为了获取不饱和烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 颜色 | B. | 质量 | C. | 压强 | D. | 密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的成分为次氯酸钙,是纯净物 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理SO2和HCl废气 | |
| D. | 干燥Cl2可使干燥有色布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | 全部 | C. | ②④⑤⑦ | D. | ①④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com