
【题目】据图回答下列问题:

(1)若烧杯中溶液为稀硫酸,则观察到的现象是_______________,电流表指针____(填“偏转”或“不偏转”),两极反应式为:正极_______________;负极______________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应方程式为______。
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示:A、B两个电极均由多孔的碳块组成。该电池的正极反应式为:___________________________。
 .
.
【答案】 镁逐渐溶解,铝上有气泡冒出 偏转 2H++2e-===H2↑ Mg-2e-===Mg2+ Al 2Al+2NaOH+2H2O===2NaAlO2+3H2↑ O2+2H2O+4e-===4OH-
【解析】根据自发的氧化还原反应能设计成原电池,失电子的一极是负极,发生氧化反应,得到电子的是正极,发生还原反应;在燃料电池中,通入正极的一极氧气,通入负极的一极氧气是燃料,负极的电极反应=总反应-正极的电极反应和。
(1)镁、铝和稀硫酸构成了原电池,自发进行的反应是镁和硫酸反应,金属镁做负极,
电极反应:Mg-2e-=Mg2+,金属铝为正极,溶液中的H+得到电子发生还原反应,电极反应为:2H++2e-=H2↑,所以可看到镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转,故答案为:镁逐渐溶解,铝极上有气泡冒出;电流表指针发生偏转;2H++2e-=H2↑;Mg-2e-=Mg2+;(2)镁、铝和氢氧化钠溶液构成了原电池,自发的氧化还原反应是金属铝和氢氧化钠之间的反应,总反应方程式为:2Al+2NaOH+2H2O===2NaAlO2+3H2↑,铝失电子,为负极,金属镁作正极;(3)氢气、氧气和氢氧化钾溶液构成了原电池,自发的氧化还原反应是氢气和氧气之间的反应,总反应方程式为:2H2+O2=2H2O,正极上通的是氧气,B极是正极,电极反应:O2+2H2O+4e-=4OH-。


科目:高中化学 来源: 题型:
【题目】圣路易斯大学研制的新型乙醇燃料电池,使用能传递质子(H+)的介质作溶剂,反应原理为C2H5OH+3O2→2CO2+3H2O,下图是该电池的示意图,下列说法正确的是

A. a极为电池的正极
B. 电池工作时,电流由a极沿导线经灯泡再到b极
C. 电池正极的电极反应为:4H++O2+4e-═2H2O
D. 电池工作时,1mol乙醇被氧化,则电路中有6mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N4分子结构为正四面体(如图所示)。已知:断裂N4(g)中1 molN-N键吸收193kJ能量,形成N2(g)中1 mol N![]() N放出941 kJ能量。下列说法正确的是
N放出941 kJ能量。下列说法正确的是

A. N4(g)比N2(g)更稳定
B. N4(g)=2N2(g) △H=+724kJmol-1
C. 形成1 mol N4(g)中的化学键放出193 kJ的能量
D. lmolN2(g)完全转化为N4(g),体系的能量增加362kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 实验室采用如图所示装置制备乙酸乙酯,实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿该试管内壁缓缓加入紫色石蕊试液1毫升,发现紫色石蕊试液存在于饱和碳酸钠溶液层与乙酸乙酯液层之间(整个过程不振荡试管),下列有关该实验的描述,不正确的是( )

A.制备的乙酸乙酯中混有乙酸和乙醇杂质
B.该实验中浓硫酸的作用是催化和吸水
C.饱和碳酸钠溶液主要作用是降低乙酸乙酯的溶解度及吸收乙醇、中和乙酸
D.石蕊层为三层环,由上而下是蓝、紫、红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物体的生命活动离不开水。下列关于水的叙述,错误的是
A. 在最基本生命系统中,H20有自由水和结合水两种存在形式
B. 由氨基酸形成多肽链时,生成物H20中的氢来自氨基和羧基
C. 玉米体细胞中含量最多的有机物是水
D. 细胞内的水能参与营养物质的运输,也能作为细胞内化学反应的反应物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.﹣CHO的电子式: ![]()
B.丙烷分子的比例模型为: ![]()
C.2﹣乙基﹣1,3﹣丁二烯的键线式: ![]()
D.对硝基甲苯的结构简式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室产生的废液中含有Fe3+、Cu2+、Ba2+、Cl﹣四种离子,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体. 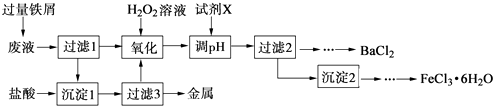
(1)沉淀1中含有的金属单质是 .
(2)氧化时加入H2O2溶液发生反应的离子方程式为 .
(3)下列物质中,可以作为试剂X的是(填字母).
A.BaCl2
B.BaCO3
C.NaOH
D.Ba(OH)2
(4)检验沉淀2洗涤是否完全的方法是 .
(5)制备氯化铁晶体过程中需保持盐酸过量,其目的是 .
(6)由过滤2得到的滤液制备BaCl2的实验操作依次为、冷却结晶、、洗涤、干燥.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com