
| A. | 蒸馏法是海水谈化的方法之一 | |
| B. | 海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料 | |
| C. | 海水中的Li元素属于微量元素,提炼后可作Li电池原料 | |
| D. | 0℃以上,温度越高,水的密度越小 |
分析 A.海水中水的沸点低于盐类物质;
B.放射性元素可释放大量的能量,可用于制造核反应堆;
C.海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料;
D.从水的密度和温度的关系角度分析.
解答 解:A.海水中水的沸点低于盐类物质,则蒸馏海水获得淡水,故A正确;
B.放射性元素可释放大量的能量,海水中的${\;}_{92}^{235}$U元素经浓缩提炼后可作核反应堆燃料,故B正确;
C.海水中的Li元素属于微量元素,海水中锂元素储量非常丰富,提炼后可作Li电池原料,故C正确;
D.水在4℃时密度最大,故D错误.
故选D.
点评 本题考查了好像知识的积累和理解应用,解答本题要掌握物质的存在状态、水的密度及水的应用等方面的内容,只有这样才能对相关方面的问题做出正确的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将氨水滴加到饱和的FeCl3溶液中并加热 |
| B | 由AlCl3溶液制备无水AlCl3 | 将AlCl3溶液加热蒸干 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | 除去HBr中混有的Br2蒸汽 | 将混合气体通入盛有CCl4的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由上述反应可知,ClO-的氧化性强于FeO42- | |
| B. | 高铁酸钾中铁显+6价 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为2:3 | |
| D. | K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
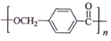 的路线:
的路线: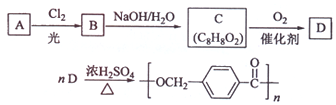
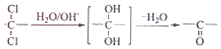
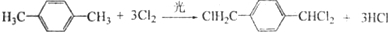 ;
;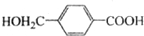 ,由D合成聚酯类高分子材料
,由D合成聚酯类高分子材料 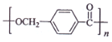 的化学方程式是n
的化学方程式是n $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +(n-1)H2O
+(n-1)H2O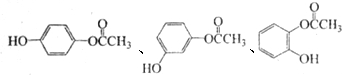 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
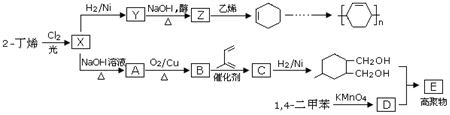
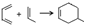 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 283kJ•mol-1 | B. | +172.5 kJ•mol-1 | C. | -172.5 kJ•mol-1 | D. | -504 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com