
| A. | 冰醋酸 | B. | 纯硫酸 | C. | 蔗糖溶液 | D. | 氢氧化钠溶液 |
分析 能导电的物质--必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子.
在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、金属氧化物和水;
在水溶液里和熔融状态下都不导电的化合物是非电解质,包括非金属氧化物、部分非金属氢化物、大多数有机物;
单质和混合物既不是电解质,也不是非电解质;
完全电离的电解质属于强电解质,部分电离的电解质属于弱电解质,包括弱酸、弱碱、水与少数盐.
解答 解:A.冰醋酸是纯净的乙酸,在溶液中部分电离,属于弱电解质,故A错误;
B.纯硫酸,因在溶液中能完全电离出自由移动的氢离子和硫酸根离子,能导电,属于强电解质,但纯硫酸只有硫酸分子,无自由移动的离子,所以属于强电解质但不导电,故B正确;
C.蔗糖溶液存在蔗糖分子,没有自由移动的离子,故不能导电,它是混合物,电解质必须是化合物,所以它不是电解质,故C错误;
D.氢氧化钠溶液,有自由移动的钠离子和氢氧根离子,能导电,但氢氧化钠溶液是混合物,所以它不是电解质,故D错误;
故选B.
点评 本题考查强弱电解质与导电之间的关系判断,明确溶液导电的原因、注意电解质的强弱是以电离程度判断的,不是以导电能力大小判断的是解答关键,题目难度不大,试题能够培养学生灵活应用所学知识的能力.


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用锌粉代替锌粒 | B. | 改用热的2 mol/L硫酸溶液 | ||
| C. | 改用3 mol/L硫酸溶液 | D. | 向该硫酸溶液中加入等体积的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铬位于元素周期表的第四周期第Ⅷ族 | |
| B. | 警察通过装有橙色的酸性重铬酸钾的装置检查司机是否酒后驾车 | |
| C. | 已知铬元素的一种同位素的质量数为53,则该同位素有53个中子 | |
| D. | 中子数为29的铬原子符号表示为${\;}_{24}^{29}$Cr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgI,AgBr,AgCl | B. | AgCl,AgI,AgBr | C. | AgBr,AgI,AgCl | D. | AgCl,AgBr,AgI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
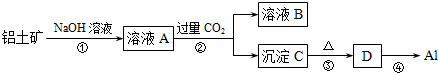
| A. | 原溶液中一定不存在Ba2+和HCO3- | |
| B. | 取③中滤液加入KSCN,溶液显红色,则原溶液一定有Fe3+ | |
| C. | 原溶液中一定存在SO42-和Cl- | |
| D. | 为确定原溶液中是否含有K+,可通过焰色反应直接观察焰色是否为紫色来确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA | |
| B. | 18g D2O含有的电子数为10NA | |
| C. | 在标准状况下,22.4LSO3的物质的量为1mol | |
| D. | 同温、同压下,相同体积的氟气和氩气所含的原子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com