
| A. | 减小、增大、减小 | B. | 增大、减小、减小 | C. | 减小、增大、增大 | D. | 增大、减小、增大 |
分析 含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.
解答 解:CH3COONa是强碱弱酸盐其水溶液呈碱性,Na2SO3是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;NH4NO3是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加硝酸铵会促进醋酸根离子水解,导致醋酸根离子浓度减小;
FeCl3是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加FeCl3会促进醋酸根离子水解,导致醋酸根离子浓度减小,
故选B.
点评 本题考查了影响盐类水解的因素,明确含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1的CH3COOH | B. | 0.1 mol•L-1的NaHSO4 | ||
| C. | 0.1 mol•L-1的NaHCO3 | D. | 0.05 mol•L-1的H2SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
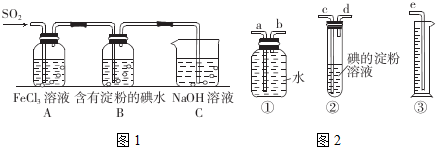
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO(g)═C(s)+$\frac{1}{2}$O2(g) | B. | 2N2O5(g)═4NO2(g)+O2(g) | ||
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g) | D. | MgCO3(s)═MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳离子只能得到电子被还原,作氧化剂 | |
| B. | 在金属活性顺序表中,Na排在Cu的前面,所以Na可与CuSO4溶液反应置换出单质Cu | |
| C. | 在氧化还原反应中,不一定所有元素的化合价都发生变化 | |
| D. | 氧化还原反应中,某元素由化合态变为游离态,此元素一定被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、NO3-、CO32- | B. | Mg2+、Na+、Cl-、SO42- | ||
| C. | Mg2+、NH4+、NO3-、CO32- | D. | NH4+、K+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不需要通过化学反应就能从海水中获得食盐和淡水 | |
| B. | 推广使用可降解塑料及布质购物袋,无法减少“白色污染” | |
| C. | 严格执行机动车尾气排入标准有利于防止大气污染 | |
| D. | 使用二氧化硫和某些含硫化合物进行增白的食品对人体健康有害 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食品包装袋中常放入小袋还原铁粉,目的是防止食品氧化变质 | |
| B. | 铝表面有一层致密的氧化膜,故铝制容器可以用来腌制咸菜等 | |
| C. | “埃博拉”病毒在常温下较稳定,对热有中等度抵抗力,56℃不能完全灭活,60℃30min方能破坏其感染性,此过程主要发生了蛋白质的变性 | |
| D. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com