
选做[有机化学]](10分)邻羟基桂皮酸(IV)是合成香精的重要原料,下列为合成邻羟基桂皮酸(IV)的路线之一
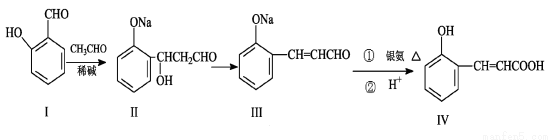
试回答:
(1)I中含氧官能团的名称 和 。
(2)II→III的反应类型 。
(3)① IV与乙醇和浓硫酸混合加热的化学方程式 。
② IV与过量NaOH溶液反应的化学方程式 。
(4)有机物X与IV互为同分异构体,且X有如下特点:
① 是苯的对位取代物, ② 能与NaHCO3反应放出气体 ,③能发生银镜反应。
请写出X的一种结构简式 。
(10分) (1)羟基 醛基 (2分) (2)消去反应(2分,)
(3)①
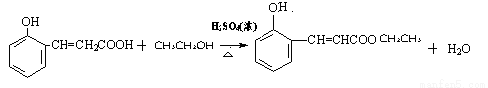
(2分,未写条件扣1分)
②
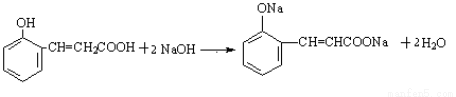
(2分,未配平扣1分)
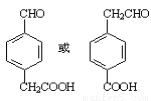 (2分,-CHO写成-COH不得分)
(2分,-CHO写成-COH不得分)
【解析】
试题分析:(1)I中含氧官能团的名称叫羟基、醛基;
(2)比较II和III的结构简式,可知发生的是醛基的消去反应,增加碳碳双键,所以II→III的反应类型是消去反应;
(3)① IV中的羧基与乙醇在浓硫酸作催化剂、加热条件下发生酯化反应,生成酯和水,化学方程式为 ;
;
②IV中的羟基、羧基均与氢氧化钠溶液反应,所以IV与过量的氢氧化钠反应的化学方程式为
(4)能与NaHCO3反应放出气体 ,说明X分子中含有羧基;能发生银镜反应,说明X分子中含有醛基,X是苯的对位取代物,说明羧基与醛基处于对位位置,按照取代基C原子的数目可知符合条件的X的结构简式是
考点:考查有机物的性质判断,官能团的判断,化学方程式的书写,同分异构体的判断


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源:2014-2015湖南省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各组离子不能大量共存的是
A.Cl-、Na+、NO3-、OH- B.HCO3-、Cl-、Na+、K+
C.Ba2+、Cl-、SO42-、K+ D.NH4+、K+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省高二上学期期中化学(文)试卷(解析版) 题型:选择题
在南方人们的主食是大米,在进食时,我们将米饭在嘴中长时间嚼为什么感觉到有甜味呢
A.淀粉在唾液淀粉酶的作用下转变成麦芽糖
B.淀粉中含有葡萄糖
C.淀粉在唾液淀粉酶的作用下转变成葡萄糖
D.淀粉是糖类物质有甜味
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
下图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是
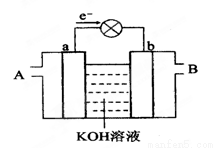
A.A处通入空气,B处通入水煤气
B.a电极的反应式包括:CO+4OH--2e-= CO32-+2H2O
C.a电极发生还原反应,b电极发生氧化反应
D.如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
某学习小组的同学查阅相关资料知氧化性:Cr2O72->Fe3+,设计了盐桥式的原电池,见下图。盐桥中装有琼脂与饱和K2SO4溶液。下列叙述中正确的是
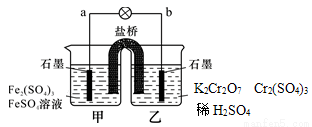
A.甲烧杯的溶液中发生还原反应
B.乙烧杯中发生的电极反应为:2Cr3++7H2O - 6e- = Cr2O72-+14H+
C.外电路的电流方向是从b到a
D.电池工作时,盐桥中的SO42- 移向乙烧杯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期第四次月考化学试卷(解析版) 题型:选择题
检验氯化氢中是否含有氯气,可采用的方法是
A.用干燥的蓝色石蕊试纸 B.用干燥的有色布条
C.将气体通入硝酸银溶液中 D.将气体通入品红溶液中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期第三次月考理综试卷(解析版) 题型:填空题
选考[化学——选修3:物质结构与性质] (15分)
锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:
2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu的第三能层的电子排布式 ,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有 (填元素符号),上述方程式中涉及到的N、O元素第一电离能由小到大的顺序为 。
(2)PO43-的空间构型是 。
(3)氨基乙酸铜的分子结构如图,氮原子的杂化方式为 。
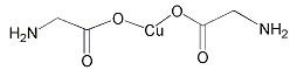
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则CN-中含有的σ键与π键的数目之比为 。
(5)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为 。
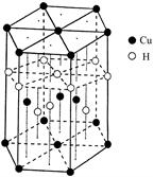
(6)铜晶体为面心立方最密堆积,铜的原子半径为r pm,则晶体铜密度的计算式为 g/cm3。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:选择题
向一定量的Cu、Fe2O3的混合物中加人600mL 2mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,再加入过量1 mol/L NaOH溶液,将沉淀过滤、洗涤、干燥,称得质量比原混合物增重17.6g,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量是
A.4.8 g B.8.8 g C.9.6g D.14.4g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com