
分析 (1)活泼金属和活泼金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物;
(2)不同非金属元素之间易形成极性键,含有空轨道和含有孤电子对的原子之间易形成配位键;
(3)同种非金属元素之间易形成非极性键,活泼金属和活泼非金属元素之间易形成离子键,含有离子键的化合物是离子化合物;
(4)含有离子键的化合物是离子化合物,不同非金属元素之间易形成极性键;
(5)同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,正负电荷重心重合的分子是非极性分子.
解答 解:①NaOH中存在极性键和离子键,属于离子化合物;
②Na2S中只含离子键,属于离子化合物;
③(NH4)2S中存在离子键、配位键和极性键,属于离子化合物;
④Na2O2中含有离子键和非极性键,属于离子化合物;
⑤C2H2中含有极性键和非极性键,属于共价化合物,且属于非极性分子;
(1)活泼金属和活泼金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物是离子化合物,所以只含有离子键的离子化合物是硫化钠,故答案为:②;
(2)不同非金属元素之间易形成极性键,含有空轨道和含有孤电子对的原子之间易形成配位键,所以含离子键、极性键和配位键的化合物是③,故答案为:③;
(3)同种非金属元素之间易形成非极性键,活泼金属和活泼非金属元素之间易形成离子键,含有离子键的化合物是离子化合物,所以含有非极性键的离子晶体是④,故答案为:④;
(4)含有离子键的化合物是离子化合物,不同非金属元素之间易形成极性键,所以含有极性键的离子晶体是①③,故答案为:①③;
(5)同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,正负电荷重心重合的分子是非极性分子,所以含有极性键和非极性键的非极性分子是⑤,故答案为:⑤.
点评 本题考查化学键,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,注意离子键和共价键的区别,注意:配位键属于共价键.


科目:高中化学 来源: 题型:选择题
| A. | 常温时,BeCl2溶液的pH>7 | |
| B. | 常温时,Na2BeO2溶液的pH<7 | |
| C. | Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 | |
| D. | BeCl2水溶液的导电性较强,说明BeCl2一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液溴应保存于带磨口玻璃塞的广口试剂瓶中,并加水“水封”以减少其易挥发 | |
| B. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | |
| C. | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ | |
| D. | 氨气是一种诚性气体,可用P2O5或无水CaCl2干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
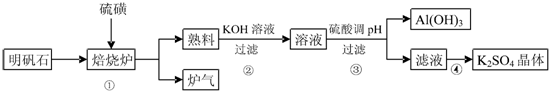
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②④⑤ | C. | ③⑤⑥ | D. | ①②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com