
| 序号 | 实验方案 | 实验现象 | 化学方程式 |
| ① | 将少量氯水加入盛有NaBr溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为橙红色 | Cl2+2NaBr=2NaCl+Br2 |
| ② | 将少量溴水加入盛有碘化钾溶液的试管中,用力振荡后加入少量四氯化碳溶液,振荡、静置 | 加入溴水后,溶液由无色变为褐色,滴入四氯化碳后,水层颜色变浅,四氯化碳层变为紫红色 |
分析 氯气具有氧化性,能将溴离子氧化为溴单质,溴单质在有机层显示橙红色;溴单质能将碘离子氧化为碘单质,碘单质在有机层中显示紫红色,据此回答.
(1)根据实验现象结合氧化剂的氧化性强于氧化产物的氧化性来得出同主族元素性质的递变规律;
(2)实验在试管内进行,移取液体时用胶头滴管;
(3)①根据实验方案可知,将氯水滴入盛有少量NaBr溶液的试管中,并做萃取实验;
②探究同一主族元素性质的递变规律,溴单质的氧化性强碘单质,将少量溴水滴入盛有少量KI溶液的试管中,产生碘单质,然后再用少量四氯化碳萃取,碘单质溶解在萃取剂四氯化碳中;
(4)氯气能将溴离子从其水溶液中置换出来,而溴单质能将碘离子从其水溶液中置换出来,说明氧化性是氯气强于溴单质,溴单质强于碘单质,元素的非金属性越强,得出同主族元素性质的递变规律;
(5)依据原子结构理论解答即可.
解答 解:(1)氯、溴、碘为同一主族元素,根据实验现象结合氧化剂的氧化性强于氧化产物的氧化性来得出同主族元素性质的递变规律,
故答案为:探究同一主族元素性质的递变规律;
(2)实验在试管内进行,移取液体时用胶头滴管,
故答案为:胶头滴管;
(3)①根据实验实验方案可知,将氯水滴入盛有少量NaBr溶液的试管中,发生反应:Cl2+2NaBr=2NaCl+Br2,并做萃取实验,滴入少量四氯化碳,振荡,四氯化碳层变为橙红色;
②溴单质的氧化性强碘单质,探究同一主族元素性质的递变规律,根据实验现象可知,需将少量溴水滴入盛有少量KI溶液的试管中,产生碘单质,然后再用少量四氯化碳萃取,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为紫红色,
故答案为;
| 序号 | 实验方案 | 实验现象 | 化学方程式 |
| ① | 橙红色 | Cl2+2NaBr=2NaCl+Br2 | |
| ② | 碘化钾 |
点评 本题考查了同主族元素性质递变规律的性质实验设计和验证,非金属得到电子的能力强弱比较方法和反应现象判断,侧重分析与实验能力的考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下NA个SO3的体积为22.4 L | |
| B. | 1 mol Fe与足量的HCl反应,转移的电子数为3NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )| A. | lg$\frac{{V}_{2}}{{V}_{1}}$=6时,HA溶液的pH=8 | |
| B. | pH相同时,c(HA)>c(HB) | |
| C. | 曲线上a、b两点 $\frac{[{B}^{-}]}{[HB][O{H}^{-}]}$ 一定不相等 | |
| D. | 25℃时,NaA溶液的pH一定小于NaB溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
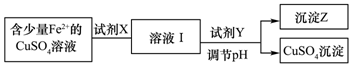
| 金属 离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.4 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
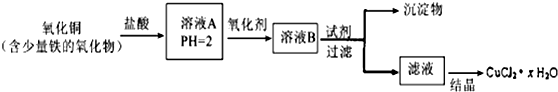
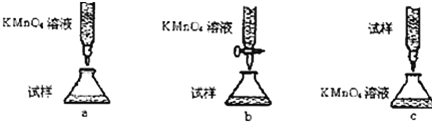
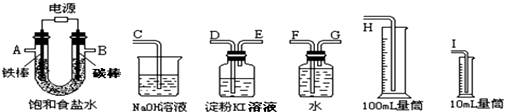
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
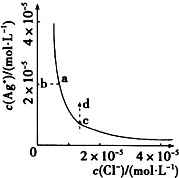 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A. | d点没有AgCl的不饱和溶液 | |
| B. | c点对应的Ksp 等于a点对应的Ksp | |
| C. | 加入AgNO3,可以使溶液由c点变到d点并保持不变 | |
| D. | 加入少量水,平衡右移,Cl- 浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
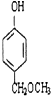
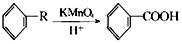 从A出发,发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体.
从A出发,发生图示中的一系列反应,其中B和C按1:2反应生成Z,F和E按1:2反应生成W,W和Z互为同分异构体.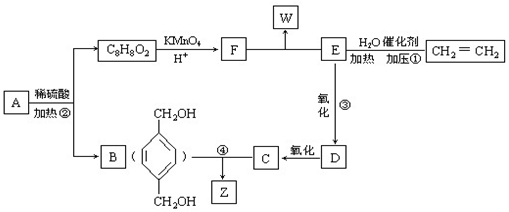
 +2CH3COOH$?_{△}^{浓硫酸}$
+2CH3COOH$?_{△}^{浓硫酸}$ +2H2O.
+2H2O.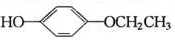 、
、 、
、 、
、 任意2个 (任写两种)
任意2个 (任写两种)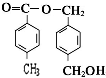 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| C. | 1molCl2参加的氧化还原反应,反应过程中转移电子数都是2NA | |
| D. | 常温常压下,92gNO2和N2O4混合气体含有的原子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 NO2与SO2能发生反应:NO2+SO2?SO3+NO,某研究小组对此进行相关实验探究.
NO2与SO2能发生反应:NO2+SO2?SO3+NO,某研究小组对此进行相关实验探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com