
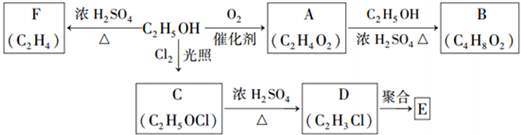
分析 乙醇被氧化生成A,且A能和乙醇反应,根据A的分子式知,A为CH3COOH,A在浓硫酸作催化剂、加热条件下发生消去反应生成F,F为CH2=CH2,乙醇和氯气在光照条件下发生取代反应生成C,C在浓硫酸作催化剂、加热条件下能发生消去反应,则C结构简式为CH2ClCH2OH、D为CH2=CHCl,D发生聚合反应生成聚氯乙烯,E结构简式为 ,A和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成B,B为CH3COOCH2CH3,以此解答该题.
,A和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成B,B为CH3COOCH2CH3,以此解答该题.
解答 解:乙醇被氧化生成A,且A能和乙醇反应,根据A的分子式知,A为CH3COOH,A在浓硫酸作催化剂、加热条件下发生消去反应生成F,F为CH2=CH2,乙醇和氯气在光照条件下发生取代反应生成C,C在浓硫酸作催化剂、加热条件下能发生消去反应,则C结构简式为CH2ClCH2OH、D为CH2=CHCl,D发生聚合反应生成聚氯乙烯,E结构简式为 ,A和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成B,B为CH3COOCH2CH3,
,A和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成B,B为CH3COOCH2CH3,
(1)A是乙酸,A的结构简式为CH3COOH,故答案为:CH3COOH;
(2)B为CH3COOCH2CH3,B的化学名称是乙酸乙酯,故答案为:乙酸乙酯;
(3)C是2-氯乙醇,含氧官能团为羟基,故答案为:羟基;
(4)E结构简式为 ,其化学名称是聚氯乙烯,故答案为:聚氯乙烯;
,其化学名称是聚氯乙烯,故答案为:聚氯乙烯;
(5)F是乙烯,乙醇在浓硫酸作催化剂、加热170℃条件下,乙醇发生消去反应生成乙烯,反应方程式为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
点评 本题考查有机物推断,侧重考查学生分析推断能力,涉及乙醇、乙烯、卤代烃、羧酸、酯、高分子化合物之间的转化,明确常见有机物官能团及其性质、常见有机反应类型及反应条件即可解答,注意乙醇制取乙烯必须控制好温度.


科目:高中化学 来源: 题型:多选题
| A. | 硝酸银和氯化钠的混合溶液 | B. | 硫酸铜和硫酸钾的混合溶液 | ||
| C. | Na2CO3和NaOH混合溶液 | D. | CuCl2和HCl混合溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷中混有的乙烯,可以用酸性KMnO4溶液洗气除去 | |
| B. | 乙烯、苯都易燃烧,燃烧时都产生明亮火焰、大量黑烟 | |
| C. | 乙酸乙酯、油脂都能水解,且在热的NaOH溶液中水解更完全 | |
| D. | 葡萄糖、淀粉都有还原性,都能与新制Cu(OH)2共热产生砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)指出下列能量的变化:
(1)指出下列能量的变化:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝制电线电缆 | B. | 铝制餐具 | C. | 铝制可乐易拉罐 | D. | 糖果内包装 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com