
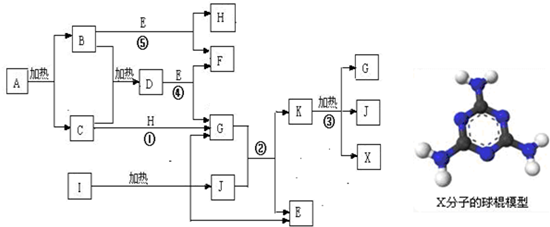
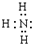 故答案为:
故答案为: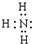 ;
; C3H6N6+6 NH3+3 CO2 ;
C3H6N6+6 NH3+3 CO2 ; C3H6N6+6 NH3+3 CO2 ;
C3H6N6+6 NH3+3 CO2 ;

科目:高中化学 来源: 题型:

| △ |
| △ |
 、
、 、
、 、
、
 、
、 、
、 、
、


查看答案和解析>>
科目:高中化学 来源: 题型:

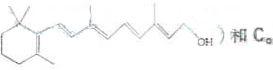 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.



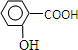





查看答案和解析>>
科目:高中化学 来源: 题型:









查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示装置中:

a是盛有标准状况下的空气(氧气占1/5)和10mL 1.2mol/L硝酸的250 mL烧瓶;b是未充气(实验开始前内部没有气体)放有0.384g铜粉的气球;c是夹紧了的弹簧夹;d中盛有足量的过氧化钠;e是充有二氧化碳的针筒。整套装置已经过气密性检查合格。
(1)将气球中的铜粉小心倒入烧杯中,充分反应后发现铜粉有余(设产生的气体不溶解于溶液中),则可观察到的现象是 。
(2)欲提高铜与硝酸反应的速率可采用多种不同的措施。
①若用加入化学试剂法,下列试剂中可以选用的是
A.蒸馏水 B. 无水醋酸钠
C.石墨 D. 少量硝酸银溶液
②若用升温法,请在图中画出完整的示意图。
③将烧瓶不断振荡发现气球逐渐缩小,反应的化学方程式是 ,
此时气球是全在烧瓶外还是一部分进入烧瓶?
④打开弹簧夹,将二氧化碳反推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉全溶解,至少需要推入二氧化碳 mL.
⑤将上述全过程用一个总的化学方程式表示: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com