


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:不详 题型:单选题
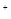 )/c(OH
)/c(OH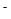 )
)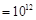 的溶液中;
的溶液中;| A.①③⑥ | B.①②④ | C.①②⑤⑦ | D.③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
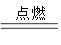 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.① | B.①③ | C.②③④⑤⑥⑦ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| a | | | |||||||||||||||
| | | | | b | c | d | e | | |||||||||
| | | | f | | | | g | | |||||||||
| | | | | | | | | | d | | h | [ | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.是一种新元素 | B.原子核内有185个质子 |
| C.原子核内有185个中子 | D.是183Hf的一种新的同位素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 序 号 | 元素 | 结构及性质 |
| ① | A | 在地壳中的含量居于第三位,单质由电解法制取,其化学性质活泼,但在空气中能稳定存在;其离子半径在同周期中金属离子中最小。 |
| ② | B | B原子最外层电子数是内层电子数的1/5 |
| ③ | C | C单质分子中含化学键数最多,单质稳定,但其原子较活泼 |
| ④ | D | 通常情况下,D没有正化合价,A、B、C、E都能与D化合 |
| ⑤ | E | E在周期表中可以排在IA族,也有人提出排在ⅦA族、ⅣA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com