
| A、乙酸乙酯 | B、乙醇 |
| C、葡萄糖 | D、乙酸 |
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
| KMnO4酸性溶液的浓度/mol?L-1[学|科| | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
| 实验编号 | 20℃下,试管中所加试剂及其用量/mL | 20℃下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 4 | 4.0 | 1.0 | 3.0 | 2.0 | 4.0 |
| 5 | 2.5 | 2.5 | 3.0 | 2.0 | 4.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子核外只有三个能级,且各能级电子数相等 |
| Y | Y的基态原子最外层电子数是其内层电子总数的2.5倍 |
| Z | Z的基态价电子结构为nsn-1 |
| W | W单质常在火山口附近被发现,其氧化物是造成酸雨的主要原因之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸钡可用于钡餐透视 |
| B、为防止电池中的重金属离子污染土壤和水源,废电池要集中处理 |
| C、明矾可用于水的消毒、杀菌 |
| D、食醋可用于除去热水瓶中的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
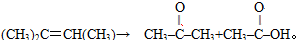 现有1mol某烯烃分子被酸性高锰酸钾溶液氧化后得到2molCO2,和
现有1mol某烯烃分子被酸性高锰酸钾溶液氧化后得到2molCO2,和 请写出该烯烃分子发生加聚反应的化学方程式
请写出该烯烃分子发生加聚反应的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在碱溶液中生成CN-和OCN- |
| B、跟卤素反应生成CNCl、CNBr等 |
| C、不能在空气中燃烧 |
| D、可与Ag反应生成可溶盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业生产玻璃、水泥、陶瓷都要使用石灰石做原料 |
| B、开发氢能、太阳能、风能、生物质能等新型能源是践行低碳生活的有效途径 |
| C、“把世博会期间产生的垃圾焚烧或深埋处理”方案符合上海世博会实现“环保世博、生态世博”的目标 |
| D、光化学烟雾、臭氧层空洞、温室效应、硝酸型酸雨的形成都与氮氧化合物有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、直径介于1nm~100nm之间的微粒称为胶体 |
| B、电泳现象可证明胶体带电荷 |
| C、利用丁达尔效应可以区别溶液与胶体 |
| D、按照分散质和分散剂状态不同(固、液、气),它们之间可有6种组合方式 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com