
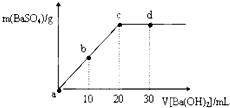
| A£® | ĮņĖįČÜŅŗµÄĢå»żĪŖ30 mL | |
| B£® | bŹ±æĢČÜŅŗÖŠSO42-µÄÅضČŌ¼ĪŖ0.125 mol•L-1 | |
| C£® | dŹ±æĢČÜŅŗµÄpHŌ¼ĪŖ13 | |
| D£® | ČÜŅŗµÄµ¼µēÄÜĮ¦£ŗc£¼d=b£¼a |
·ÖĪö A£®ĮņĖįŗĶĒāŃõ»Æ±µČÜŅŗ·“Ó¦·½³ĢŹ½ĪŖH2SO4+Ba£ØOH£©2=BaSO4”ż+2H2O£¬¶žÕßŅŌ1£ŗ1·“Ó¦£¬ĒŅc£ØH2SO4£©=c[Ba£ØOH£©2]£¬¶žÕßĶźČ«·“Ó¦Ź±ĻūŗĵÄĢå»żĻąµČ£¬øł¾ŻĶ¼ÖŖ£¬¼ÓČėĒāŃõ»Æ±µ20mLŹ±¶žÕßĒ”ŗĆ·“Ó¦£¬ĖłŅŌV£ØH2SO4£©=V[Ba£ØOH£©2]=20mL£»
B£®bŹ±æĢSO42-³ĮµķŅ»°ė£¬Ģå»ż±äĪŖŌĄ“µÄ1.5±¶£¬²Ī¼Ó·“Ó¦µÄĮņĖįøłĄė×ÓŹĒŌĄ“ČÜŅŗÖŠÅØ¶ČµÄŅ»°ė£»
C£®dŹ±æĢ£¬ČÜŅŗÖŠµÄČÜÖŹŹĒBa£ØOH£©2£¬c£ØOH-£©=$\frac{0.25”Į10”Į2}{50}$mol/L=0.1mol/L£»
D£®ČÜŅŗÖŠĄė×ÓÅضČŌ½“óĘäµē½āÖŹČÜŅŗµ¼µēŠŌŌ½Ē森
½ā“š ½ā£ŗA£®ĮņĖįÓėĒāŃõ»Æ±µ·¢ÉśÖŠŗĶ·“Ó¦£¬CµćĒ”ŗĆ·“Ó¦ĶźČ«£¬ŅņĪŖ¶žÕßÅضČĻąĶ¬£¬ĖłŅŌĢå»żĻąµČĪŖ20mL£¬¹ŹA“ķĪó£»
B£®bŹ±æĢSO42-³ĮµķŅ»°ė£¬Ģå»ż±äĪŖŌĄ“µÄ1.5±¶£¬SO42-µÄÅضČŌ¼ĪŖ$\frac{0.25mol/L”Į0.5}{1.5}$mol/L=0.083mol•L-1£¬¹ŹB“ķĪó£»
C£®dŹ±æĢBa£ØOH£©2¹żĮ棬c£ØOH-£©=$\frac{0.25”Į10”Į2}{50}$mol/L=0.1mol/L£¬ŌņpH=13£¬¹ŹCÕżČ·£»
D£®b”¢dĮ½µćĄė×ÓĪļÖŹµÄĮæĻąµČ£¬µ«ŗóÕßĢå»ż“ó£¬Ąė×ÓÅØ¶ČŠ”£¬µ¼µēŠŌČõ£¬µ¼µēÄÜĮ¦c£¼d£¼b£¼a£¬¹ŹD“ķĪó£»¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó·½³ĢŹ½µÄÓŠ¹Ų¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬Ć÷Č·Ķ¼ÖŠø÷µć·¢ÉśµÄ·“Ó¦¼°ČÜŅŗÖŠµÄČÜÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄѵćŹĒÅŠ¶ĻČÜŅŗµ¼µēÄÜĮ¦“󊔣¬ŅדķŃ”ĻīŹĒD£®


 ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø
ĆūŠ£ĮŖĆĖæģĄÖæĪĢĆĻµĮŠ“š°ø »ĘøŌ““ÓžķĻµĮŠ“š°ø
»ĘøŌ““ÓžķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŃĪĖį | B£® | ĪŽĖ®ŅŅ“¼ | C£® | ŹÆ»ŅĖ® | D£® | H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
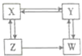 X”¢Y”¢Z”¢WĪŖ“¼”¢Č©”¢Ėį”¢õ„ÖŠµÄŅ»ÖÖ£¬ĖüĆĒÖ®¼ä“ęŌŚČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
X”¢Y”¢Z”¢WĪŖ“¼”¢Č©”¢Ėį”¢õ„ÖŠµÄŅ»ÖÖ£¬ĖüĆĒÖ®¼ä“ęŌŚČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | XŹĒōČĖį£¬YŹĒõ„ | B£® | YŹĒČ©£¬WŹĒ“¼ | C£® | ZŹĒČ©£¬WŹĒōČĖį | D£® | XŹĒ“¼£¬ZŹĒõ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĖįÓėĢ¼ĖįÄĘČÜŅŗ·“Ó¦£ŗ2H++CO32-ØTCO2”ü+H2O | |
| B£® | “×ĖįČÜŅŗÓėŠĀÖĘĒāŃõ»ÆĶ·“Ó¦ 2CH3COOH+Cu£ØOH£©2ØT£ØCH3COO£©2Cu+2 H2O | |
| C£® | ±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĢ¼£ŗ2C6H5O-+CO2+H2OØT2C6H5OH+CO32- | |
| D£® | AlCl3ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++3NH3•H2OØTAl£ØOH£©3”ż+3NH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
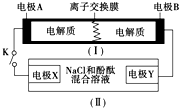 ĻĀĶ¼ĪŖŅ»ÖÖæɳäµēµē³ŲµÄŹ¾ŅāĶ¼£¬ĘäÖŠµÄĄė×Ó½»»»Ä¤Ö»ŌŹŠķK+Ķعż£¬øƵē³Ų·Åµē”¢³äµēµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2K2S2+KI3 $?_{³äµē}^{·Åµē}$K2S4+3KI£®×°ÖĆ£Ø¢ņ£©ĪŖµē½ā³ŲµÄŹ¾ŅāĶ¼£®µ±±ÕŗĻæŖ¹ŲKŹ±£¬µē¼«Xø½½üČÜŅŗĻȱäŗģ£®Ōņ±ÕŗĻKŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ĻĀĶ¼ĪŖŅ»ÖÖæɳäµēµē³ŲµÄŹ¾ŅāĶ¼£¬ĘäÖŠµÄĄė×Ó½»»»Ä¤Ö»ŌŹŠķK+Ķعż£¬øƵē³Ų·Åµē”¢³äµēµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ2K2S2+KI3 $?_{³äµē}^{·Åµē}$K2S4+3KI£®×°ÖĆ£Ø¢ņ£©ĪŖµē½ā³ŲµÄŹ¾ŅāĶ¼£®µ±±ÕŗĻæŖ¹ŲKŹ±£¬µē¼«Xø½½üČÜŅŗĻȱäŗģ£®Ōņ±ÕŗĻKŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | K+“Ó×óµ½ÓŅĶعżĄė×Ó½»»»Ä¤ | |
| B£® | µē¼«AÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ3I--2e-ØTI3- | |
| C£® | µē¼«XÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗ2Cl--2e-ØTCl2”ü | |
| D£® | µ±ÓŠ0.1 mol K+ĶعżĄė×Ó½»»»Ä¤£¬Xµē¼«ÉĻ²śÉś1.12 LĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆÄĘČÜŅŗÓĆ“ų²£Į§ČūµÄ²£Į§Ęæ“ę·Å | |
| B£® | ½šŹōÄʱ£“ęŌŚĖ®ÖŠ | |
| C£® | ÅØĻõĖį“ę·ÅÓŚĪŽÉ«ĻøæŚĘæÖŠ | |
| D£® | ÅØĮņĖįÖü“ęŌŚĀĮÖĘČŻĘ÷ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol H2SO4Óė1 molBa£ØOH£©2·“Ӧɜ³ÉH2OŹ±·Å³öµÄČČ½Š×öÖŠŗĶČČ | |
| B£® | ”÷H£¾0 kJ•mol-1±ķŹ¾·ÅČČ·“Ó¦£¬”÷H£¼0 kJ•mol-1±ķŹ¾ĪüČČ·“Ó¦ | |
| C£® | ČČ»Æѧ·½³ĢŹ½ÖŠµÄ»Æѧ¼ĘĮæŹż±ķŹ¾ĪļÖŹµÄĮ棬æÉŅŌŹĒ·ÖŹż | |
| D£® | 1 mol H2Óė0.5 mol O2·“Ó¦·Å³öµÄČČ¾ĶŹĒH2µÄČ¼ÉÕČČ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com