
【题目】航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
水电解反应:2H2O(l)![]() 2H2(g)+O2(g)
2H2(g)+O2(g)
(1)将原料气按![]() ∶
∶![]() =1∶4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
=1∶4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
① 该反应的平衡常数K随温度升高而__________(填“增大”或“减小”)。

② 温度过高或过低均不利于该反应的进行,原因是________。
③ 200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为________。(不必化简。用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化效率的是______(填标号)。
A.适当减压
B.增大催化剂的比表面积
C.反应器前段加热,后段冷却
D.提高原料气中CO2所占比例
E.合理控制反应器中气体的流速
(3)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)![]() C(s)+2H2O(g)代替Sabatier反应。
C(s)+2H2O(g)代替Sabatier反应。
① 已知CO2(g)、H2O(g)的生成焓分别为–394 kJmol-1、–242 kJmol-1,Bosch反应的ΔH =________kJmol-1。(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
② 一定条件下Bosch反应必须在高温下才能启动,原因是________。
③ 新方案的优点是________。
【答案】 减小 温度过低,反应速率减小 温度过高,反应向右进行的程度小 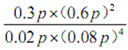 BCE -90 反应的活化能高;氢原子利用率为100%。
BCE -90 反应的活化能高;氢原子利用率为100%。
【解析】(1)①根据H2O(g)的物质的量分数与温度的关系图可得:温度越高,H2O(g)的物质的量分数越低,故随升高温度该反应的平衡常数K减小。②温度过低,反应速率很小;温度过高,反应向右进行的程度小,故温度过高或过低均不利于该反应的进行。③200℃时平衡体系中H2O(g)的物质的量分数为0.6,根据反应化学方程式CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),所以CH4的物质的量分数为0.3,因此CO2和H2的物质的量分数共为0.1,又因为原料气按
CH4(g)+2H2O(g),所以CH4的物质的量分数为0.3,因此CO2和H2的物质的量分数共为0.1,又因为原料气按![]() ∶
∶![]() =1∶4置于密闭容器中发生Sabatier反应,所以CO2的物质的量分数为0.02,H2的物质的量分数为0.08;达到平衡时体系的总压强为p,则四种物质的分压分别为:p(CO2)=0.02p、p(H2)=0.08p、p(CH4)=0.3p、p(H2O)=0.6p,所以该反应平衡常数Kp为:
=1∶4置于密闭容器中发生Sabatier反应,所以CO2的物质的量分数为0.02,H2的物质的量分数为0.08;达到平衡时体系的总压强为p,则四种物质的分压分别为:p(CO2)=0.02p、p(H2)=0.08p、p(CH4)=0.3p、p(H2O)=0.6p,所以该反应平衡常数Kp为:![]() =
=![]() 。
。
(2)首先明确:转化效率不等于转化率。A项,适当减压化学反应速率降低、降低平衡转化率,故A错误;B项,增大催化剂的比表面积,提高了化学反应速率,能提高CO2转化效率,故B正确;C项,反应器前段加热,加快反应速率,后段冷却,提高平衡转化率,故C正确;D项,提高原料气中CO2所占比例,降低CO2的转化率,故D错误;E项,合理控制反应器中气体的流速,可使反应物充分反应,提高了CO2转化效率,故E正确。综上,选BCE。
(3)①由已知可得:C(s)+O2(g)=CO2(g) ΔH =–394 kJmol-1,2H2(g)+O2(g)=2H2O(g) ΔH =–484 kJmol-1,所以Bosch反应CO2(g)+2H2(g)![]() C(s)+2H2O(g)的ΔH=[–484-(-394)] kJmol-1=-90kJmol-1。②Bosch反应为放热反应,一定条件下必须在高温下才能启动,说明高温条件才能引发此反应开始,故该反应的活化能很高。③新方案与原方案相比氢原子利用率为100%。
C(s)+2H2O(g)的ΔH=[–484-(-394)] kJmol-1=-90kJmol-1。②Bosch反应为放热反应,一定条件下必须在高温下才能启动,说明高温条件才能引发此反应开始,故该反应的活化能很高。③新方案与原方案相比氢原子利用率为100%。


科目:高中化学 来源: 题型:
【题目】已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)![]() CO2(g)+H2(g),在427 ℃时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01 mol/ L,
CO2(g)+H2(g),在427 ℃时的平衡常数是9。如果反应开始时,一氧化碳和水蒸气的浓度都是0.01 mol/ L,
(1)计算一氧化碳在此反应条件下的转化率_____________。
(2)若将一氧化碳和水蒸气的浓度都变为0.02 mol/ L,其它条件不变,则达到平衡时,求H2的物质的量浓度_____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸生产中炉气转化反应为2SO2(g)+O2(g)![]() 2SO3(g)。研究发现,SO3的体积分数 (SO3%)随温度(T)的变化如曲线I所示。下列判断不正确的是
2SO3(g)。研究发现,SO3的体积分数 (SO3%)随温度(T)的变化如曲线I所示。下列判断不正确的是

A. 该反应的正反应为放热反应
B. 曲线I上A、C两点反应速率的关系是:VA<VC
C. 反应达到B点时,2V正(O2) = V逆(SO3)
D. 已知V2O5的催化效果比Fe2O3好,若I表示用V2O5作催化剂的曲线,则Ⅱ可表示用Fe2O3作催化剂的曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某元素的原子核外电子排布中,K电子层和L电子层的电子数之和等于M电子层和N电子层的电子数之和。则该元素的核电荷数为
A. 12 B. 17 C. 20 D. 30
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有相同质子数和电子数的两种微粒之间的关系不正确的是:
A. 它们可能是同位素 B. 可能是不同的分子
C. 可能是不同的离子 D. 可能是一种分子和一种离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A、B、C、D、E之间的转化关系如图所示。

已知:
回答下列问题:
(l)A中含有的官能团名称为_________。
(2)由C 生成D 的反应类型为________。
(3)X 的结构简式为_________。
(4)由D 生成E 的化学方程式为_________。
(5)F是D的同分异构体,符合下列条件的F 的结构共有________种(不考虑立体异构)。
①能与NaHCO3溶液发生反应 ②能与FeCl3溶液发生显色反应 ③苯环上只有2个取代基
(6)写出以环戊烷和2-丁烯为原料(其他无机试剂任选)制备化合物![]() 的合成路线_______。
的合成路线_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“宏观﹣微观﹣符号”三重表征是化学独特的表示物质及其变化的方式,请结合图回答下列问题:
(1)图1中,“Cu”表示多种信息,如表示铜元素、铜单质,还能表示;
(2)从微粒的角度说明图2反应的实质是;
(3)图3为物质甲发生分解反应的微观示意图.①物质甲中氧元素的化合价为;
②写出反应的化学方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砹(At)是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是
A. 砹易溶于某些有机溶剂 B. 砹化氢很稳定不易分解
C. 砹是有色气体 D. 砹化银不溶于水或稀HNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com