
| A£® | ĪåÖÖŌŖĖŲµÄŌ×Ó°ė¾¶“ӓ󵽊”µÄĖ³ŠņŹĒ£ŗZ£¾W£¾M£¾Y£¾X | |
| B£® | Ēā»ÆĪļµÄ»¹ŌŠŌ£ŗY£¾M£¾W | |
| C£® | YŗĶMµÄŃõ»ÆĪļ¶¼ŹĒĖįŠŌŃõ»ÆĪļ | |
| D£® | X2ZµÄµē×ÓŹ½ĪŖ£ŗ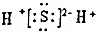 |
·ÖĪö X”¢Y”¢Z”¢W”¢MŹĒ¶ĢÖÜĘŚ5ÖÖÖ÷×åŌŖĖŲ£¬X-Óėŗ¤Ō×Óµē×Ó²ć½į¹¹ĻąĶ¬£¬ŌņXŹĒHŌŖĖŲ£»YŌ×ӵĵē×Ó×ÜŹżµČÓŚĘäµē×Ó²ćŹżµÄ3±¶£¬YĪŖCŌŖĖŲ£»ZµÄ×īøß»ÆŗĻ¼ŪĪŖ×īµĶ»ÆŗĻ¼Ū¾ų¶ŌÖµµÄ3±¶£¬ZĪŖSŌŖĖŲ£»WµÄµ„ÖŹæÉÓėÄĘ·“Ӧɜ³ÉŅõŃōĄė×ÓøöŹż±ČĪŖ1£ŗ2µÄµ»ĘÉ«¹ĢĢå»ÆŗĻĪļ£¬ŌņWĪŖOŌŖĖŲ£»MµÄĒā»ÆĪļÓėĘä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļæÉ·¢Éś»ÆŗĻ·“Ӧɜ³ÉŃĪ£¬MĪŖNŌŖĖŲ£¬
A£®ŌŖĖŲŌ×Óµē×Ó²ćŹżŌ½¶ąĘäŌ×Ó°ė¾¶Ō½“ó£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ£¬Ō×Ó°ė¾¶Ėę×ÅŌ×ÓŠņŹżŌö“ó¶ų¼õŠ”£»
B£®ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Čõ£¬ĘäĒā»ÆĪļµÄ»¹ŌŠŌŌ½Ē棻
C£®Y”¢MŹĒC”¢NŌŖĖŲ£¬CO”¢NOŹĒ²»³ÉŃĪŃõ»ÆĪļ£»
D£®H2SŹĒ¹²¼Ū»ÆŗĻĪļ£¬ĆæøöHŌ×ÓŗĶSŌ×ÓÖ®¼äŠĪ³É¹²¼Ū¼ü£®
½ā“š ½ā£ŗX”¢Y”¢Z”¢W”¢MŹĒ¶ĢÖÜĘŚ5ÖÖÖ÷×åŌŖĖŲ£¬X-Óėŗ¤Ō×Óµē×Ó²ć½į¹¹ĻąĶ¬£¬ŌņXŹĒHŌŖĖŲ£»YŌ×ӵĵē×Ó×ÜŹżµČÓŚĘäµē×Ó²ćŹżµÄ3±¶£¬YĪŖCŌŖĖŲ£»ZµÄ×īøß»ÆŗĻ¼ŪĪŖ×īµĶ»ÆŗĻ¼Ū¾ų¶ŌÖµµÄ3±¶£¬ZĪŖSŌŖĖŲ£»WµÄµ„ÖŹæÉÓėÄĘ·“Ӧɜ³ÉŅõŃōĄė×ÓøöŹż±ČĪŖ1£ŗ2µÄµ»ĘÉ«¹ĢĢå»ÆŗĻĪļ£¬ŌņWĪŖOŌŖĖŲ£»MµÄĒā»ÆĪļÓėĘä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļæÉ·¢Éś»ÆŗĻ·“Ӧɜ³ÉŃĪ£¬MĪŖNŌŖĖŲ£¬
A£®ŌŖĖŲŌ×Óµē×Ó²ćŹżŌ½¶ąĘäŌ×Ó°ė¾¶Ō½“ó£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ£¬Ō×Ó°ė¾¶Ėę×ÅŌ×ÓŠņŹżŌö“ó¶ų¼õŠ”£¬Ō×Ó°ė¾¶“óŠ”Ė³ŠņŹĒS£¾C£¾N£¾O£¾H£¬¼“Z£¾Y£¾M£¾W£¾X£¬¹ŹA“ķĪó£»
B£®ŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Čõ£¬ĘäĒā»ÆĪļµÄ»¹ŌŠŌŌ½Ē棬·Ē½šŹōŠŌW£¾M£¾Y£¬ĖłŅŌĒā»ÆĪļµÄ»¹ŌŠŌW£¼M£¼Y£¬¹ŹBÕżČ·£»
C£®Y”¢MŹĒC”¢NŌŖĖŲ£¬CO”¢NOŹĒ²»³ÉŃĪŃõ»ÆĪļ£¬¹ŹC“ķĪó£»
D£®H2SŹĒ¹²¼Ū»ÆŗĻĪļ£¬ĆæøöHŌ×ÓŗĶSŌ×ÓÖ®¼äŠĪ³É¹²¼Ū¼ü£¬Ęäµē×ÓŹ½ĪŖ £¬¹ŹD“ķĪó£»
£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ŗĶŌŖĖŲÖÜĘŚĀɵĹŲĻµ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜ·ÖĪöÅŠ¶ĻÄÜĮ¦£¬Éę¼°ŌŖĖŲÖÜĘŚĀÉ”¢»Æѧ¼üµČÖŖŹ¶µć£¬Ć÷Č·ŌŖĖŲÖÜĘŚ±ķ½į¹¹”¢Ō×Ó½į¹¹¼°ŌŖĖŲÖÜĘŚĀÉŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢Ņā¹ęĀÉÖŠµÄ·“³£ĻÖĻó£¬ŅדķŃ”ĻīŹĒC£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŅŃÖŖ£ŗ·“Ó¦I£ŗ4NH3£Øg£©+6NO£Øg£©?5N2£Øg£©+6H2O£Øl£©”÷H1
ŅŃÖŖ£ŗ·“Ó¦I£ŗ4NH3£Øg£©+6NO£Øg£©?5N2£Øg£©+6H2O£Øl£©”÷H1| ĪĀ¶Č/K | ·“Ó¦I | ·“Ó¦II | ŅŃÖŖ£ŗ K2£¾K1 £¾K2”䣾K1”ä |
| 298 | K1 | K2 | |
| 398 | K1ӊ | K2ӊ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ²£Į§°ō | B£® |  ¾Ę¾«µĘ | C£® | 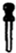 ½ŗĶ·µĪ¹Ü | D£® |  ČŻĮæĘæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹŌ¹Ü”¢Õō·¢Ćó¼ČÄÜÓĆÓŚøų¹ĢĢå¼ÓČČŅ²ÄÜÓĆÓŚøųČÜŅŗ¼ÓČČ | |
| B£® | ·ÖŅŗĀ©¶·¼ČÄÜÓĆÓŚÄ³Š©»ģŗĻĪļµÄ·ÖĄėŅ²ÄÜÓĆÓŚ×é×°ĘųĢå·¢Éś×°ÖĆ | |
| C£® | ¼īŹ½µĪ¶Ø¹Ü¼ČæÉÓĆÓŚÖŠŗĶµĪ¶Ø£¬Ņ²æÉÓĆÓŚĮæČ”Ņ»¶ØĮæµÄNaCl»ņAlCl3ČÜŅŗ | |
| D£® | ²āĮæ¾Ę¾«·ŠµćµÄŹµŃéÖŠ£¬Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņĪ»ÓŚ±»¼ÓČČµÄ¾Ę¾«ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÕāÖÖĮ£×ÓÖŠŗ¬ÓŠ3øöÖŹ×Ó | B£® | ĖüµÄ×é³ÉæÉÓĆH3±ķŹ¾ | ||
| C£® | ÕāÖÖĮ£×ÓÖŠŗ¬ÓŠ3øöÖŠ×Ó | D£® | ŹĒĒāµÄŅ»ÖÖŠĀµÄĶ¬Ī»ĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
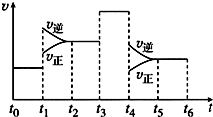 300”ęĻĀ£¬½«2mol SO21mol O2»ģŗĻÓŚ2LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¬2·ÖÖÓÄ©“ļµ½Ę½ŗā£¬²āµĆSO2µÄ×Ŗ»ÆĀŹĪŖ60%£¬Ēėøł¾Ż»Æѧ·“Ó¦µÄÓŠ¹ŲŌĄķ»Ų“šĻĀĮŠĪŹĢā£ŗ
300”ęĻĀ£¬½«2mol SO21mol O2»ģŗĻÓŚ2LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¬2·ÖÖÓÄ©“ļµ½Ę½ŗā£¬²āµĆSO2µÄ×Ŗ»ÆĀŹĪŖ60%£¬Ēėøł¾Ż»Æѧ·“Ó¦µÄÓŠ¹ŲŌĄķ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
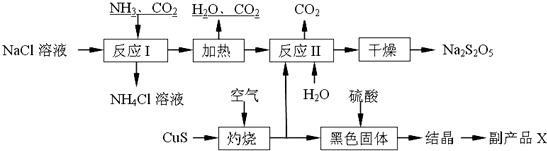
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
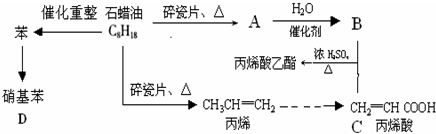
 A”śBµÄ·“Ó¦ĄąŠĶ£ŗ¼Ó³É·“Ó¦
A”śBµÄ·“Ó¦ĄąŠĶ£ŗ¼Ó³É·“Ó¦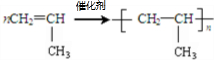 £»
£»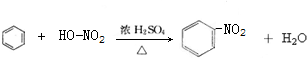 £¬
£¬²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
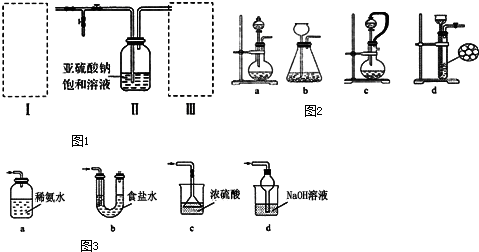
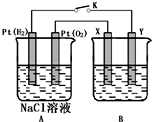 ij»ÆѧŠĖȤŠ”×éÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠµē»ÆѧŌĄķµÄŹµŃéĢ½¾æ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
ij»ÆѧŠĖȤŠ”×éÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠµē»ÆѧŌĄķµÄŹµŃéĢ½¾æ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com