
(14分)某学习小组用下图装置测定镁铝合金中铝的质量分数和铝的相对原子质量。
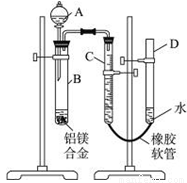
(1)A中试剂为______________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤、洗涤、干燥,称重;
③待B中不再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B中滴加足量试剂。
上述操作的顺序是___________(填序号);在进行操作③时记录C的液面位置时,除视线平视外,还应_ 。
(4)B中发生反应的化学方程式为___________________。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为_______________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________(填“偏大”、“偏小”、“无影响”)。
(14分,每空2分) (1)NaOH溶液 (2)除去铝镁合金表面的氧化膜
(3)①④③②,使D和C的液面相平 (4) 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(5) 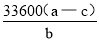 (6)偏小
(6)偏小
【解析】
试题分析:(1)由于B中有固体剩余,这说明加热的试剂不是酸,而氢氧化镍,镁与氢氧化钠不反应,铝与氢氧化钠溶液反应生成偏铝酸钠和氢气。
(2)由于镁铝均是活泼的金属,在其表面有氧化膜,则实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是除去铝镁合金表面的氧化膜。
(3)实验前首先记录C中液面位置,然后加入氢氧化钠溶液,当不再有气体产生时再记下液面位置,最后将B中剩余固体过滤、洗涤、干燥,称重,所以上述操作的顺序是①④③②。由于气体的体积受压强的影响,所以再记录液面时还需要使D和C的液面相平。
(3)氢氧化钠溶液与铝反应,镁不反应,则B中反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
(4)氢气的物质的量是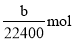 ,则根据方程式可知需要金属铝的物质的量是
,则根据方程式可知需要金属铝的物质的量是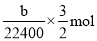 。合金中铝的质量是(a—c)g,则铝的相对原子质量是
。合金中铝的质量是(a—c)g,则铝的相对原子质量是 。
。
(5)实验过程中,若未洗涤过滤所得的不溶物,则剩余固体质量偏大,即c偏大,所以测得铝的质量分数将偏小。
考点:考查物质含量测定实验方案设计与探究


科目:高中化学 来源:2014-2015学年山西省晋中市高三1月考前适应性训练理综化学试卷(解析版) 题型:选择题
下列的图示与对应的传述相符的是
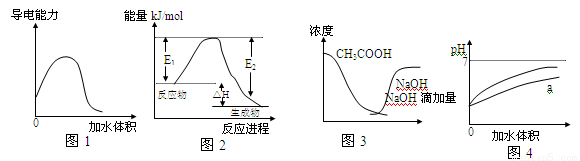
A.图1表示稀释冰醋酸过程中溶液导电性的变化曲线
B.图2表示某一放热反应,若使用催化剂E1、E2,△H都会发生改变
C.图3曲线表示将氢氧化钠滴加到醋酸溶液浓度的变化趋势
D.图4表示pH相同的盐酸与醋酸分别加入水中后溶液pH的变化,其中曲线a对应的是盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列示意图与对应的反应情况正确的是
A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2
B.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
C.NaHSO4溶液中逐滴加入Ba(OH)2溶液
D.NaAlO2溶液中逐滴加入稀盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
硅被誉为无机非金属材料的主角。据2001年12月的《参考消息》报道,有科学家提出硅是“21世纪的能”、“未的石油”。下列有关说法正确的是
A.硅在地壳中含量居第二位,在地球上有丰富的硅资,如石英、水晶、玛瑙的主要成分都是单质硅
B.在野外,用硅、烧碱的混合物可以制取氢气
C.硅的性质稳定,不与任何酸反应
D.硅是一种良好的半导体材料,所以是制造光导纤维的基本原料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.将0.1 molFeCL3溶液于1 L水中,所得溶液含Fe3+离子数目为0.1 NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA
D.在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:填空题
【物质结构与性质】(15分)钙的化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔.请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为___________________.
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的π键数目为_________.
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N).丙烯腈分子中碳原子轨道杂化类型是_______________,构成丙烯腈元素中第一电离能最大的是__________.
(2)抗坏血酸钙的组成为Ca(C6H7O6)2?4H2O,其结构示意图如图1:

该物质中存在的化学键类型包括____________(填字母).
A.金属键 B.离子键 C.非极性共价键 D.配位键
(3)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图2所示:由此可判断该钙的氧化物的化学式为____________.已知阿伏加德罗常数为NA,该晶体的密度为ρg·cm3,则晶胞中两Ca2+间的最近距离为______________cm.(用含NA、ρ的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:填空题
(12分)钛酸钡粉体是电子陶瓷元器件的重要基础原料。工业以草酸盐共沉淀法获得草酸氧钛钡晶体[BaTiO(C2O4)2·4H2O],煅烧可获得钛酸钡粉体。
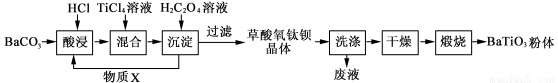
(1)酸浸时发生的反应的离子方程式为 ;为提高BaCO3的酸浸率,可采取的措施为 (任答一点)。
(2)配制TiCl4溶液时,通常将TiCl4溶于浓盐酸,目的是 。
(3)加入H2C2O4溶液时,发生反应的化学方程式为 ;
可循环使用的物质X是 。
(4)煅烧得到BaTiO3的同时,生成高温下的气体产物有CO、 和 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:实验题
(15分)碘化钠是实验室中常见的分析试剂,常用于医疗和照相业。工业上通常用水合肼(N2H4·H2O,100℃以上分解)还原法制取碘化钠,工艺流程如下:
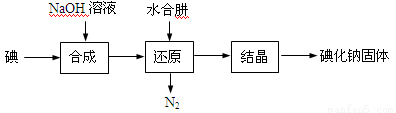
(1)合成过程的反应产物中含有IO3-,写出合成过程的离子方程式 。
(2)还原过程必须保持反应温度在60~70℃,这个温度既能保证反应的快速进行,又能 。工业上也可以用Na2S或Fe屑还原制备碘化钠,但水合肼还原法制得的产品纯度更高,原因是 。
(3)请补充完整检验还原液中是否含有IO3-的实验方案:取适量还原液, 。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液。
(4)测定产品中NaI含量的实验步骤如下:
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中;
c.用0.1000mol·L-1AgNO3溶液滴定至终点,记录消耗AgNO3溶液的体积;
d.重复b、c操作2~3次,记录相关实验数据。
①滴定过程中,AgNO3溶液应放在 中;步骤d的目的是 。
②若用上述方法测定产品中的NaI含量偏低(忽略测定过程中的误差),其可能的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com