
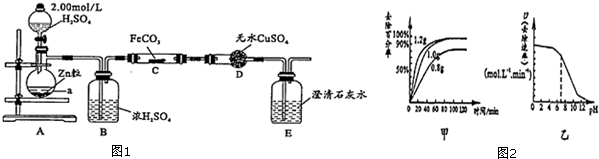
分析 (1)根据仪器的构造可知a为蒸馏烧瓶,C中的反应不能有水,浓硫酸的作用即为干燥氢气;
(2)根据反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应是氢气还原FeCO3生成铁、二氧化碳和水;
(3)将酒精灯换成酒精喷灯,D中变蓝,E中有气泡但未出现浑浊,说明产生了水和一氧化碳,可能是温度过高二氧化碳和氢气反应生成了CO;
(4)①根据图象,从反应的速率和对氯硝基苯去除百分率分析;
②当PH变大后,溶液呈碱性,会使二价铁离子沉淀为Fe(OH)2,覆盖在铁粉表面,阻碍反应进行.
解答 解:(1)根据仪器的构造可知a为蒸馏烧瓶,A中制备氢气,用氢气还原C中的铁,氢气必须干燥,浓硫酸的作用即为干燥氢气,
故答案为:蒸馏烧瓶;干燥氢气;
(2)根据反应一段时间后D中变蓝,E中溶液变浑浊,C中发生反应是氢气还原FeCO3生成铁、二氧化碳和水,化学方程式是FeCO3+H2=Fe+CO2+H2O,
故答案为:FeCO3+H2=Fe+CO2+H2O;
(3)将酒精灯换成酒精喷灯,D中变蓝,E中有气泡但未出现浑浊,说明产生了水和一氧化碳,可能是温度过高二氧化碳和氢气反应生成了CO,
故答案为:温度升高,CO2被H2还原为CO;
(4)①根据图象,在相同时间内,加入米铁粉为1.0g时,反应的速率比较快,且对氯硝基苯去除百分率比较高,而加入1.2g时当随着时间推移,去除率变化不大,速率与1.0相差不大,但是原料的费用高,加入0.8g时,速率慢、去除率低,故最佳为1.0g,
故答案为:1.0;
②当PH变大后,溶液呈碱性,会使二价铁离子沉淀为Fe(OH)2,覆盖在铁粉表面,阻碍反应进行,反应速率变化很快变小,
故答案为:PH变大,生成Fe(OH)2覆盖在铁粉表面,阻碍反应进行.
点评 本题考查了用氢气和碳酸亚铁制取纳米级铁粉,涉及到实验仪器装置的使用,物质性质的考查,反应速率的影响条件比较等广泛内容,需要对知识的全面掌握,理清实验原理,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )| A. | 在 FeBr3的催化作用下可与溴水发生取代反应 | |
| B. | 该烃与足量 H2的加成产物一氯代物最多有四种 | |
| C. | 分子中至少有10个碳原子处于同一平面上 | |
| D. | 该烃是苯的同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇 | B. | 甲酸 | C. | 甲醛 | D. | 甲酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738kJ•mol-1 I2=1451kJ•mol-1 I3=7733kJ•mol-1 I4=10540kJ•mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中未成对电子最多的元素 |
| G的3d能级只含有2对成对电子 |
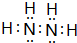 .
. 该同学所画的电子排布图违背了泡利原理.
该同学所画的电子排布图违背了泡利原理.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1 mol KClO3参加反应,有2 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
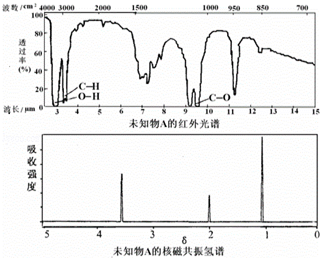
| A. | 由红光外谱可知,该有机物中有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有两种不同化学环境的氢原子 | |
| C. | 仅由核磁共振氢谱即可得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
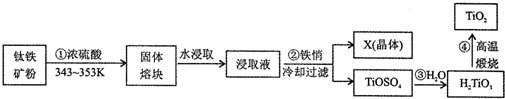
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
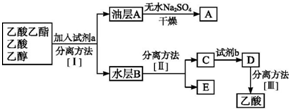 实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品.
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com