
 如图表示可逆反应A(g)+B(g)?3C(g)(正反应为放热反应),在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线,有关叙述一定正确的是( )
如图表示可逆反应A(g)+B(g)?3C(g)(正反应为放热反应),在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线,有关叙述一定正确的是( )科目:高中化学 来源: 题型:
 如图表示可逆反应mA(g)+nB(g)?pC(g)在不同温度(T)、压强(P)下,生成物C的质量分数C%的变化情况.下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是( )
如图表示可逆反应mA(g)+nB(g)?pC(g)在不同温度(T)、压强(P)下,生成物C的质量分数C%的变化情况.下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
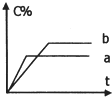 如图表示可逆反应:A(s)+B(g)?nC(g);△H=Q,在不同条件下反应混合物中C的百分含量(C%)和反应过程所需时间(t)的关系曲线.下列有关叙述中一定正确的是( )
如图表示可逆反应:A(s)+B(g)?nC(g);△H=Q,在不同条件下反应混合物中C的百分含量(C%)和反应过程所需时间(t)的关系曲线.下列有关叙述中一定正确的是( )| A、若只使用催化剂,则a表示使用了催化剂,b表示没有使用催化剂 | B、若只控制温度,则a比b的温度高,且△H>0 | C、若只控制压强,则a比b的压强大,且n>2 | D、由图象可以作出判断,反应一定从正反应方向开始 |
查看答案和解析>>
科目:高中化学 来源:2006年化学高考最后10天精题精练 题型:021
|
如图表示可逆反应A(g)+B(g)
| |
A. |
a表示有催化剂,而b无催化剂 |
B. |
若其他条件相同,a比b的温度高 |
C. |
若其他条件相同,a比b的压强大,n>2 |
D. |
反应由逆反应方向开始 |
查看答案和解析>>
科目:高中化学 来源:2012届湖北省襄樊四中高三11月月考化学试卷 题型:单选题
如图表示可逆反应A(s)+B(g)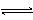 nC(g);ΔH=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述中一定正确的是
nC(g);ΔH=Q(n为正整数)在不同条件下反应混合物中C的百分含量和反应过程所需时间的关系曲线。下列有关叙述中一定正确的是
| A.其他条件相同,a表示使用了催化剂,b没有使用催化剂 |
| B.其他条件相同,若只改变温度,则a比b的温度高且ΔH>0 |
| C.其他条件相同,若只改变压强,则a比b的压强大且n≥2 |
| D.其他条件相同,若改变A的物质的量,则a比b消耗A的物质的量少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com