
����Ŀ��ij��Һ�п��ܺ���OH����CO ![]() ��AlO2����SiO
��AlO2����SiO ![]() ��SO42����HCO3����Na+��Fe3+��Mg2+��Al3+�����ӣ��������Һ����μ���һ�����ʵ���Ũ�ȵ�������Һʱ���������ɳ��������ʵ�����������Һ������仯��ͼ����ͼ��ʾ������˵����ȷ���ǣ� ��
��SO42����HCO3����Na+��Fe3+��Mg2+��Al3+�����ӣ��������Һ����μ���һ�����ʵ���Ũ�ȵ�������Һʱ���������ɳ��������ʵ�����������Һ������仯��ͼ����ͼ��ʾ������˵����ȷ���ǣ� �� 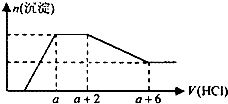
A.ԭ��Һ��һ�����е��������ǣ�OH����SiO ![]() ��AlO
��AlO ![]() ��CO
��CO ![]()
B.��Ӧ����γɵ���Һ�е�����ΪNaCl
C.ԭ��Һ��һ������Na2SO4
D.ԭ��Һ�к���CO ![]() ��AlO
��AlO ![]() ?�����ʵ���֮��Ϊ1��2
?�����ʵ���֮��Ϊ1��2
���𰸡�A
���������⣺��ͼ�������֪����ʼ��������˵��������������Һ�еļӦ��˵����Һ��һ����OH�����ӣ��������������Ӳ��ܹ��������ΪFe3+��Mg2+��Al3+�����Ӧ���ɳ���������˵����AlO ![]() ��SiO
��SiO ![]() �������ӷ�Ӧ�����������������������������AlO
�������ӷ�Ӧ�����������������������������AlO ![]() ��HCO
��HCO ![]() ������Ӧ����������������������Һ��һ��������HCO
������Ӧ����������������������Һ��һ��������HCO ![]() ����������������������䣬�������������ֻ����CO
����������������������䣬�������������ֻ����CO ![]() ���ӣ���Ӧ�������������ᣬ������С�������ٸı䣬��һ��֤��������������������������������������������ᣬ���ʣ�����Ϊ�����������Ӳ���ȷ�����ڣ���������Һ�ĵ����Կ�֪����Һ��һ������Na+���ӣ� A�������ж�ԭ��Һ��һ�����е��������ǣ�OH����SiO
���ӣ���Ӧ�������������ᣬ������С�������ٸı䣬��һ��֤��������������������������������������������ᣬ���ʣ�����Ϊ�����������Ӳ���ȷ�����ڣ���������Һ�ĵ����Կ�֪����Һ��һ������Na+���ӣ� A�������ж�ԭ��Һ��һ�����е��������ǣ�OH����SiO ![]() ��AlO
��AlO ![]() ��CO
��CO ![]() ����A��ȷ��
����A��ȷ��
B����Ӧ����γɵ���Һ�е�����ΪNaCl��AlCl3 �� ��B����
C����Һ����������Ӳ���ȷ����ʣ��ԭ��Һ����һ������Na2SO4 �� ��C����
D������ͼ���֪��̼������ӷ�Ӧ������Ϊ2�����CO ![]() +2H+=CO2��+H2O ���������ܽ����ĵ��������Ϊ4�����Al��OH��3+3H+=Al3++3H2O��ԭ��Һ�к���CO
+2H+=CO2��+H2O ���������ܽ����ĵ��������Ϊ4�����Al��OH��3+3H+=Al3++3H2O��ԭ��Һ�к���CO ![]() ��AlO
��AlO ![]() �����ʵ���֮��Ϊ3��4����D����
�����ʵ���֮��Ϊ3��4����D����
��ѡA��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���������Ƽ����ڿ����е�ȼ�ղ���A�ֱ���뵽����ˮ�У����ɵ�����������һ��������ǡ����ȫ��Ӧ������ˮ��Ӧ�Ľ������뱻������A�Ľ����Ƶ�������Ϊ
A. 1�U1 B. 2�U1 C. 23�U78 D. 46�U78
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����ʡ���;��ȷ����
A.Ũ���ᡢŨ���ᶼ����ǿ�����ԣ�����ʢ���ڽ���������
B.Na2SiO3���Ʊ��轺��ľ�ķ������ԭ��
C.ʳ�ο�����ζ����������������
D.�Ͻ��Ӳ�ȴ��۵�Ҳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����Ϊ����������ֲ��ø�������Ӽ�����չ�˲���ø�����ɸѡ��ø�Ĺ̶����������Է����о�������������ͼ��ʾ����ش�
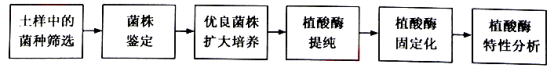
��1��������ҺŢ�Ⱦ�80������15���ӣ���Ŀ����ɸѡ��
��2�����������£�������������������Һ���� ��Ȼ��Ϳ���ں���ֲ���ƵĹ����������ϡ�������۲쵽 ������Χ������ˮ��Ȧ��Ȧ��ֱ����С�� ǿ����ء�
��3��ɸѡ��õľ��꾭�����������������Һ����������������ʱ��Ҫ������ҪĿ���� ��Һ���������������������Ȳ����еijɷ��� ��
��4���ں��������£����ᴿ��ֲ��ø�뺣�����ƻ�Ϻμӵ�һ��Ũ�ȵĸ�������Һ�У�ʹҺ���γ���������С�ù����Ƕ�ø���� ��
A������ B������ C��װ�� D��ϴ��
��5���¶���ֲ��ø���ø���ԵĹ�ϵ��ͼ��ʾ����������������� ��
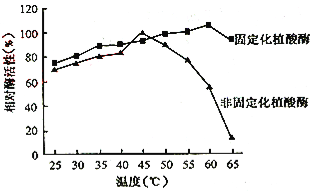
A�������¶��У��̶�����ǹ̶���ֲ��ø�������¶ȷֱ�Ϊ60����45��
B�������¶ȷ�Χ�ڣ��̶���ֲ��ø�����ø���Բ������ڷǹ̶���ֲ��ø
C���̶�����ǹ̶���ֲ��ø��ȣ����ø������80%����ʱ���¶ȷ�Χ�Ͽ�
D��65��ʱ�̶�����ǹ̶���ֲ��ø�����ø�������ʱ��Զ�λ����͵�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ��װ����������CO2��CO���岢���ͼ��aΪֹˮ�У�bΪ��Һ©���Ļ�����ͨ��Y �ܺ�ֹˮ�зֱ��c��d ������װ���ڵĿ������ž���Ϊʹʵ��ɹ����ס��ҡ����ֱ�ʢ�ŵ���Һ�ǣ� �� 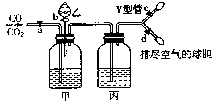
A.����NaHCO3 ��Һ��12molL��1���ᡢ18.4molL��1H2SO4
B.����Na2CO3 ��Һ��2molL��1 H2SO4������NaOH ��Һ
C.����NaOH ��Һ��2molL��1 H2SO4��18.4molL��1H2SO4
D.18.4molL��1H2SO4������NaOH ��Һ��18.4molL��1H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ħ��������˾������һ���Լ״�Ϊԭ�ϣ���KOHΪ����ʵ������ֻ��Ŀɳ��ĸ�Чȼ�ϵ�أ���һ�ε��������ʹ��һ���£���֪�õ�ص��ܷ�ӦʽΪ��2CH3OH+3O2+4KOH ![]() 2K2CO3+6H2O ����գ�
2K2CO3+6H2O ����գ�
��1���ŵ�ʱ�������ĵ缫��ӦʽΪ ��
��2��ͨ��״�һ�˵ĵ缫����������ڷŵ��������Һ��pH����������������½������䡱����
��3�����ڳ��¡���ѹ�£�1g CH3OHȼ������CO2��Һ̬ˮʱ�ų�22.68kJ����������ʾ�÷�Ӧ���Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ø�����������о��й㷺��Ӧ�ã�ͼ�ױ�ʾ��������ø����������ˮ���ģ�ͣ�ͼ�ұ�ʾ�������¶Ⱥ�pH�����£���������ø�Ĵ�����������������Ĺ�ϵ����ش��������⣺

��1����������ø��_________�кϳɣ�ͼ1ģ���ܺܺõؽ�����ø����___________�����ԣ���
��2��ͼ2�У����pH�ֱ����ߺͽ��ͣ�������ʽ��ֱ�_______��_______����������������������������������
��3�������ù�������ø��̽���¶ȶ�ø���Ե�Ӱ�죬�������ԭ��_________________��
��4�������ⶨ��������ø������pH��6.0��8.0֮�䣬��Ҫд���ⶨ��������ø����pH��ʵ��˼·_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ksp��CaSO4��=9��10��6 �� ������CaSO4��ˮ�еij����ܽ�ƽ��������ͼ�������жϴ�����ǣ� �� 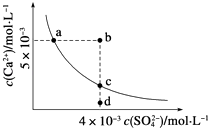
A.a��c��������Ա�ʾ������CaSO4����ˮ���γɵı�����Һ
B.a���Ӧ��Ksp����c���Ӧ��Ksp
C.b�㽫�г������ɣ�ƽ�����Һ��c��SO42����һ��������3��10��3 molL��1
D.��d����Һ�м�������CaCl2������Ա䵽c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�����CO��CO2������Oԭ�Ӹ���֮�� �� ��ͬ��ͬѹ�µ����֮�� �� ��100ml Al2��SO4��3��Һ�У� mol Al2��SO4��3�к�0.6molSO ![]() �����к�Al3+��������ȡ��10ml�ĸ���Һ��ϡ�͵�100ml����ϡ�ͺ����Һ��SO
�����к�Al3+��������ȡ��10ml�ĸ���Һ��ϡ�͵�100ml����ϡ�ͺ����Һ��SO ![]() �����ʵ���Ũ��Ϊ ��
�����ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com