
| A. | 1L 0.1mol/L的醋酸溶液含有0.1nA个H+ | |
| B. | 1molSiO2与足量的焦炭高温下完全反应生成硅,转移4nA个电子 | |
| C. | 标准状况下,11.2L H2O含有共价键的数目为nA | |
| D. | 常温常压下,14 g 由N2与C2H4组成的混合气体含有的原子数目为nA |
分析 A、醋酸是弱电解质,不能完全电离;
B、SiO2与足量的焦炭反应后硅元素的价态变为0价;
C、标况下,水为液态;
D、N2与C2H4的摩尔质量均为28g/mol,但氮气是双原子分子,而乙烯是6原子分子.
解答 解:A、醋酸是弱电解质,不能完全电离,故溶液中的氢离子的个数小于0.1nA个,故A错误;
B、SiO2与足量的焦炭反应后硅元素的价态变为0价,故1molSiO2转移4mol电子,故B正确;
C、标况下,水为液态,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、N2与C2H4的摩尔质量均为28g/mol,则14g混合气体的物质的量n=$\frac{14g}{28g/mol}$=0.5mol,但由于氮气是双原子分子,而乙烯是6原子分子,故0.5mol混合气体中的原子的物质的量介于1mol-3mol,即原子个数介于NA-3NA之间,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意的是弱电解质不能完全电离.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:选择题
| D | ||
| A | B | C |
| E |
| A. | 5Z | B. | 5Z+8 | C. | 5Z+10 | D. | 5Z+18 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.010mol/(L•s) | B. | v(O2)=0.10mo1/(L•s) | ||
| C. | v(NO)=0.10mo1/(L•s) | D. | v(H2O)=0.30mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
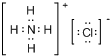 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸和氢氧化钡溶液反应 | B. | 稀硝酸与氢氧化钠溶液反应 | ||
| C. | 醋酸与氢氧化钾溶液反应 | D. | 盐酸与氢氧化铁反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 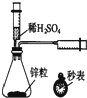 测定一定时间内生成H2的反应速率 | B. | 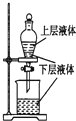 提取海带中的碘 | ||
| C. |  检验火柴燃烧产生的SO2 | D. | 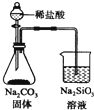 证明非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D是由短周期元素形成的单质.B、E均为组成空气的成分.化合物F的焰色反应呈黄色.在G中,非金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
A、B、C、D是由短周期元素形成的单质.B、E均为组成空气的成分.化合物F的焰色反应呈黄色.在G中,非金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出): .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com