
【题目】(1)分别取等质量的甲烷和A(饱和一元醇)、B(饱和一元醛)、C(稠环芳香烃含氧衍生物),若它们完全燃烧,生成等物质的量的CO2,则:
①A的分子式为_______________;B的分子式为_______________;C的分子式为_____________(C写出分子量最小的一种)。
②写出符合上述要求时,CH4和A、B、C的分子组成必须满足的条件是_______________(以n表示碳原子数,m表示氧原子数,只写通式)。
(2)已知:在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸,![]() 基被氧化成酮。回答下列问题:
基被氧化成酮。回答下列问题:
①1mol某烯与酸性高锰酸钾反应后生成2mol丁酮,则该烯的结构简式为是____。
②1mol某烯与酸性高锰酸钾反应后只生成1mol HOOC-CH(CH3)-CH2-CH2-CH(CH3)-COCH3,则该烯的结构简式为___(键线式表示)。
(3)某有机化合物,经测定其蒸汽是相同条件下氢气密度的30倍。取该有机物样品0.90 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重0.54 g和1.32 g.则该有机物的分子式为______。
(4)写出一氯代物只有两种的苯的同系物的结构简式并用系统命名法命名(写出两种)。
①结构简式:__________,名称:___________。
②结构简式:____________,名称:___________。
【答案】C9H20O C8H16O C10H8O2 CnH4n-16mOm CH3-CH2C(CH3)=C(CH3)CH2—CH3 ![]() C2H4O2
C2H4O2 ![]() 1,4-二甲苯
1,4-二甲苯  或
或 1,3,5-三甲苯或1,2,4,5-四甲基苯
1,3,5-三甲苯或1,2,4,5-四甲基苯
【解析】
(1)①根据A是饱和一元醇、B是饱和一元醛,设出A、B的分子式,然后利用A、B分子中含碳量与甲烷的相同列式确定二者的分子式;
②质量相同时设出的二氧化碳的物质的量相同,说明有机物分子中含有的碳元素的质量分数相同;
(2)①根据在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,![]() 基被氧化成酮分析;
基被氧化成酮分析;
②在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸分析;
(3)根据与氢气密度的关系求出该化合物的相对分子质量,浓硫酸增重0.54g为水的质量,碱石灰增重1.32g为生成的二氧化碳的质量,根据n=![]() 计算有机物、二氧化碳、水的物质的量,进而计算n(C)、n(H),根据质量守恒计算n(O),再根据原子守恒计算有机物分子中C、H、O的物质的量,书写有机物的分子式;
计算有机物、二氧化碳、水的物质的量,进而计算n(C)、n(H),根据质量守恒计算n(O),再根据原子守恒计算有机物分子中C、H、O的物质的量,书写有机物的分子式;
(4)苯的同系物只含有1个苯环,侧链为烷基,一氯代物只有两种,说明分子中只有2种不同的H原子,然后根据苯的同系物的命名方法命名;
(1)相同质量的甲烷和有机物A、B,跟氧气分别完全燃烧后,生成的二氧化碳的物质的量都相同,说明A、B含碳的质量分数与甲烷的相同。
又知A是饱和一元醇,其分子式符合CnH2n+2O,则:![]() ,解得n=9,所以A的分子式通式是C9H20O;
,解得n=9,所以A的分子式通式是C9H20O;
有机物B是饱和一元醛,其分子式符合CnH2nO,则:![]() ,解得n=8,所以B的分子式通式是C8H16O;
,解得n=8,所以B的分子式通式是C8H16O;
若C是相对分子质量最小的稠环芳香烃的含氧衍生物,则其为C10H8的含氧衍生物,假设含有的O原子数为x,即分子式为C10H8Ox,若它完全燃烧生成的CO2与等质量的CH4相等,则两者碳的质量分数相同:![]() ,解得x=2,因此C的分子式是C10H8O2;
,解得x=2,因此C的分子式是C10H8O2;
②若有机物A、B、C质量相同时完全燃烧产生的CO2与甲烷相同,说明说明有机物A、B、C分子中含碳的质量分数与甲烷的相同,有机物A、B、C分子中的H、O两种元素的含量与甲烷中的H元素的含量相同,以n表示碳原子数,m表示氧原子数,通式为CnH4n-16mOm;
(2)①根据在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,![]() 基被氧化成酮,1mol某烯与酸性高锰酸钾反应后生成2mol丁酮,说明烯烃分子中碳碳双键的两端的C原子数都为4个,不饱和C原子分别连接了一个甲基,一个乙基,该烯烃结构简式为
基被氧化成酮,1mol某烯与酸性高锰酸钾反应后生成2mol丁酮,说明烯烃分子中碳碳双键的两端的C原子数都为4个,不饱和C原子分别连接了一个甲基,一个乙基,该烯烃结构简式为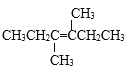 ;
;
②由于在酸性高锰酸钾溶液中氧化,烯烃分子中碳碳双键完全断裂,CH2=基被氧化成CO2,RCH=基被氧化成羧酸,1mol某烯与酸性高锰酸钾反应后只生成1mol HOOC-CH(CH3)-CH2-CH2-CH(CH3)-COCH3,将-COOH的 C=O及酮基的C=O的氧原子去掉,使2个C原子形成C、C双键,则该烯的结构简式键线式表示为![]() ;
;
(3)经测定其蒸汽是相同条件下氢气密度的30倍,则相对分子质量是氢气的30倍,所以其相对分子质量为:M=30×2=60;n(有机物)=![]() =0.015mol,n(C)=n(CO2)=
=0.015mol,n(C)=n(CO2)=![]() =0.03mol,m(C)=0.03mol×12g/mol=0.36 g,n(H)=2n(H2O)=2×
=0.03mol,m(C)=0.03mol×12g/mol=0.36 g,n(H)=2n(H2O)=2×![]() =0.06mol,m(H)=0.06mol×1g/mol=0.06g,故m(O)=0.90g-0.36 g-0.06g=0.48g,n(O)=
=0.06mol,m(H)=0.06mol×1g/mol=0.06g,故m(O)=0.90g-0.36 g-0.06g=0.48g,n(O)=![]() =0.03mol,所以该有机物分子中:N(C)=
=0.03mol,所以该有机物分子中:N(C)=![]() =2,N(H)=
=2,N(H)=![]() =4,N(O)=
=4,N(O)=![]() =2,因此有机物的分子式是 C2H4O2;
=2,因此有机物的分子式是 C2H4O2;
(4)苯的同系物只含有1个苯环,侧链为烷基,一氯代物只有两种,说明只有2种H原子,则与苯互为同系物且一氯代物只有2种的物质的结构简式为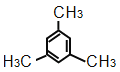 ,名称为1,3,5-三甲苯;
,名称为1,3,5-三甲苯;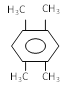 ,名称为1,2,4,5-四甲基苯。
,名称为1,2,4,5-四甲基苯。


科目:高中化学 来源: 题型:
【题目】有机物G结构简式如图所示,下列说法错误的是

A. G的分子式为C10H11O2Br
B. G能使酸性高锰酸钾溶液褪色
C. G一定条件下可以发生消去反应
D. 1molG最多能与2molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海洋资源获得的部分物质如下图所示,有关说法正确的是
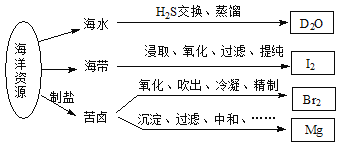
A. 在化学反应中,![]() H2O可转变为D2O
H2O可转变为D2O
B. “加碘食盐”生产中碘添加剂为单质I2
C. 实验室用带玻璃塞的棕色瓶贮存液Br2
D. 电解饱和MgCl2溶液时在阴极得到Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98 g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示;另外,某同学绘制了三条表示金属氧化物与其所含金属元素质量的关系曲线,如图2所示。则下列分析正确的是( )
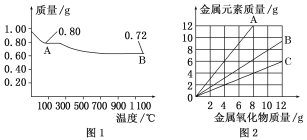
A. 图1中,A到B的过程中有0.005 mol电子发生了转移
B. 图1整个过程中共生成0.18 g水
C. 图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A
D. 图1中A和B化学式分别为Cu2O和CuO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50 mL KMnO4标准溶液的过程示意图。
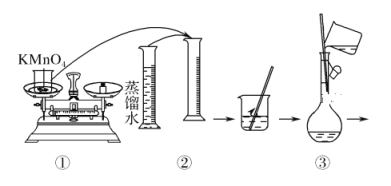
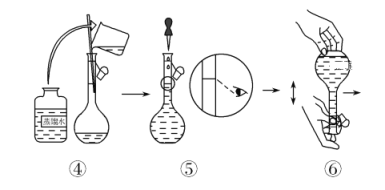
(1)请你观察图示判断,其中不正确的操作有(填序号)________。
(2)其中确定50 mL溶液体积的容器是(填名称)________。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)已知草酸跟KMnO4溶液反应的离子方程式为:
2MnO4-+5H2C2O4+6H+===2Mnx++10CO2↑+8H2O则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________mg/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)在![]() H、
H、![]() H、
H、![]() H、
H、![]() Mg、
Mg、![]() Mg和
Mg和![]() Cu中共有______种元素,______种原子
Cu中共有______种元素,______种原子
(2)下列各组微粒:①16O2和18O2 ②H2和D2 ③1735Cl和1737Cl ④1H218O和2H216O属于同位素的是___________________
(3)下列物质中:H2O2、KCl、Na2SO4、Na2O2、HCl、O2; 其中只含离子键的是________ ,只含极性键的是______ ,既含离子键又含极性键的是_____,既含离子键又含非极性键的是_______
(4)写出下列物质的电子式:Na2O2 :______________ H2O2 :________________
(5)用电子式表示下列化合物的形成过程
H2S:__________________________________
KCl:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宁夏的硒砂瓜现今已享誉区内外,西瓜富含硒元素,有延年益寿、抗衰老、抗癌作用,因之得名“硒砂瓜”。二氧化硒(Se)是一种氧化剂,其被还原后的单质硒,可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程当中涉及到如下两个化学反应:①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O。下列有关叙述正确的是
A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2
B.①中Se是氧化产物,I2是还原产物
C.反应②中方框中的物质为还原产物
D.反应①中每有0.6mol I2生成,转移电子数目为2.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是( )

选项 | 气体 | a | b | c | d |
A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO溶液 | 浓硫酸 |
B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应:X2(g)+3Y2(g) 2Z2(g)在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是

A.t2~t3时,各物质的浓度不再发生变化
B.t2时,反应未达到限度
C.t2~t3时,反应已停止进行
D.t1时,反应只向正反应方向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com