
����Ŀ��̼��������Ҫ�ķǽ���Ԫ�أ����������������й㷺��Ӧ�á�
(1)��ֲ֪�������÷����ķ�Ӧ���£�6CO2(g)��6H2O(l) ![]() C6H12O6(s)��6O2(g) ��H����669.62 kJmol��1�÷�Ӧ�ﵽ��ѧƽ������ı�����������CO2ת�����������__________��
C6H12O6(s)��6O2(g) ��H����669.62 kJmol��1�÷�Ӧ�ﵽ��ѧƽ������ı�����������CO2ת�����������__________��
a������CO2��Ũ�� b��ȡ��һ��C6H12O6
c��������� d���ʵ������¶�
(2)N2O5�ķֽⷴӦ2N2O5(g)![]() 4NO2(g) + O2(g)����ʵ������67��ʱN2O5��Ũ����ʱ��ı仯���£�
4NO2(g) + O2(g)����ʵ������67��ʱN2O5��Ũ����ʱ��ı仯���£�
ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 |
c(N2O5) /(molL��1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
������0��2minʱ�Σ���ѧ��Ӧ����v(NO2) ��________molL-1min-1��
(3)����NO2��O2ͨ�������Ƴ���ͼ��ʾװ�ã�D�缫���к�ɫ������������A�缫��ͨ�������Ϊ_________���ѧʽ����A�缫�ĵ缫��ӦʽΪ_______________________��һ��ʱ������������0.2 mol Cu(OH)2ʹ��Һ��ԭ����ת�Ƶĵ��ӵ����ʵ���Ϊ _____________��
(4)����CO��NO����ͬ����Ͷ��һ�ܱ������з�����Ӧ��2CO(g)��2NO(g)![]() N2(g)��2CO2(g)����H����759.8 kJ��mol��1����Ӧ�ﵽƽ��ʱ��N2�����������n(CO)/n(NO)�ı仯��������ͼ
N2(g)��2CO2(g)����H����759.8 kJ��mol��1����Ӧ�ﵽƽ��ʱ��N2�����������n(CO)/n(NO)�ı仯��������ͼ
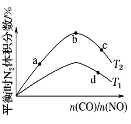
��b��ʱ��ƽ����ϵ��C��Nԭ�Ӹ���֮�Ƚӽ�________________��
��a��b��c����CO��ת���ʴӴ�С��˳��Ϊ____________��a��c��d�����ƽ�ⳣ���Ӵ�С��˳��Ϊ__________________��
����![]() ��0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����CO��ת����Ϊ___________��
��0.8����Ӧ��ƽ��ʱ��N2���������Ϊ20%����CO��ת����Ϊ___________��
���𰸡�d 0.5 NO2 NO2��e-��H2O=NO3-��2H�� 0.8 mol 1��1 a>b>c a��c>d 75%
��������
��1��a������CO2��Ũ�ȣ���Ӧ��Ũ������ƽ��������Ӧ�����ƶ�����CO2��ת���ʼ�С��
b���ı������������ܸı䷴Ӧ���ʣ����ܸı�ƽ����ƶ�����
c�������ܽ��ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ����ܸı�ƽ����ƶ�����
d���÷�ӦΪ���ȷ�Ӧ���ʵ������¶ȣ�ƽ��������Ӧ�����ƶ���
��2���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿɵ�v(NO2) ��2v(N2O5)��
��3����D�缫���к�ɫ����������֪���׳�Ϊȼ�ϵ�أ�ͨ�����������һ��Ϊ����������Cu��OH��2ʹ��Һ��ԭ˵�����������ȵ������ͭ��Һ������ͭ��Һ��ȫ����������˲���ˮ��
��4����b��ʱ��N2��������������Ӧ������ʵ���֮�Ƚӽ����ڻ�ѧ������֮�ȣ�
������Ӧ��CO��Ũ�ȣ�ƽ��������Ӧ�����ƶ���NO��ת��������CO��ת���ʼ�С����ͼ��֪��![]() ��ֵ���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����ѧƽ�ⳣ����С��
��ֵ���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����ѧƽ�ⳣ����С��
�������⽨������ʽ���ɵá�
��1��a������CO2��Ũ�ȣ���Ӧ��Ũ������ƽ��������Ӧ�����ƶ�����CO2��ת���ʼ�С���ʴ���
b���ı������������ܸı䷴Ӧ���ʣ����ܸı�ƽ����ƶ�������ȡ��һ��C6H12O6��ƽ�ⲻ�ƶ���CO2��ת���ʲ��䣬�ʴ���
c�������ܽ��ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ����ܸı�ƽ����ƶ���������������ƽ�ⲻ�ƶ���CO2��ת���ʲ��䣬�ʴ���
d���÷�ӦΪ���ȷ�Ӧ���ʵ������¶ȣ�ƽ��������Ӧ�����ƶ���CO2��ת����������ȷ��
d��ȷ���ʴ�Ϊ��d��
��2���ɱ������ݿ�֪��0��2min��N2O5��Ũ�ȱ仯Ϊ��1.00��0.50��mol/L=0.50mol/L����v(N2O5) ��![]() =0.25 molL-1min-1���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿɵ�v(NO2) ��2v(N2O5) ��
=0.25 molL-1min-1���ɻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿɵ�v(NO2) ��2v(N2O5) ��![]() ��2=0.5molL-1min-1���ʴ�Ϊ��0.5��
��2=0.5molL-1min-1���ʴ�Ϊ��0.5��
��3����D�缫���к�ɫ����������֪���׳�Ϊȼ�ϵ�أ�ͨ�����������һ��Ϊ��������A��ͨ����������������������£����������ڸ���ʧȥ���ӷ���������Ӧ�������ᣬ�缫��ӦʽΪNO2��e-��H2O=NO3-��2H�����������ͭ��Һ�Ļ�ѧ����ʽΪ2CuSO4+2H2O��![]() 2Cu��+O2��+2H2SO4���ɷ���ʽ��֪��Ӧ��ֻ����Ҫ����CuO��CuCO3�Ϳ���ʹ��Һ��ԭ������Cu��OH��2ʹ��Һ��ԭ˵�����������ȵ������ͭ��Һ������ͭ��Һ��ȫ����������˲���ˮ�����ʱ������ʼ����OH���ŵ磬�缫��ӦʽΪ4OH����4e��=2H2O+O2����������ͭ��0.2mol���������ԭ���غ��֪����Ӧ��ת�Ƶĵ�����0.2mol��2��2��0.8mol���ʴ�Ϊ��NO2��NO2��e-��H2O=NO3-��2H����0.8 mol��
2Cu��+O2��+2H2SO4���ɷ���ʽ��֪��Ӧ��ֻ����Ҫ����CuO��CuCO3�Ϳ���ʹ��Һ��ԭ������Cu��OH��2ʹ��Һ��ԭ˵�����������ȵ������ͭ��Һ������ͭ��Һ��ȫ����������˲���ˮ�����ʱ������ʼ����OH���ŵ磬�缫��ӦʽΪ4OH����4e��=2H2O+O2����������ͭ��0.2mol���������ԭ���غ��֪����Ӧ��ת�Ƶĵ�����0.2mol��2��2��0.8mol���ʴ�Ϊ��NO2��NO2��e-��H2O=NO3-��2H����0.8 mol��
��4����b��ʱ��N2��������������Ӧ������ʵ���֮�Ƚӽ����ڻ�ѧ������֮�ȣ��ɻ�ѧ����ʽ��֪��C��Nԭ�Ӹ���֮�Ƚӽ�1:1���ʴ�Ϊ��1:1��
������Ӧ��CO��Ũ�ȣ�ƽ��������Ӧ�����ƶ���NO��ת��������CO��ת���ʼ�С����ͼ��֪��![]() ��ֵ���� a��b��c����CO��ת���ʳʼ�С���ƣ���a>b>c���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����ѧƽ�ⳣ����С����ͼ��֪��N2���������T1>T2����Ӧ�¶�T2>T1���¶Ȳ���ƽ�ⳣ�����䣬a��c�ķ�Ӧ�¶���ͬ����С��d����ƽ�ⳣ��a��c>d���ʴ�Ϊ��a>b>c��a��c>d��
��ֵ���� a��b��c����CO��ת���ʳʼ�С���ƣ���a>b>c���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ�����ѧƽ�ⳣ����С����ͼ��֪��N2���������T1>T2����Ӧ�¶�T2>T1���¶Ȳ���ƽ�ⳣ�����䣬a��c�ķ�Ӧ�¶���ͬ����С��d����ƽ�ⳣ��a��c>d���ʴ�Ϊ��a>b>c��a��c>d��
����![]() ��0.8����CO�����Ϊ0.8L��NO���Ϊ1L��CO��ת����Ϊa�������⽨����������ʽ��
��0.8����CO�����Ϊ0.8L��NO���Ϊ1L��CO��ת����Ϊa�������⽨����������ʽ��

��N2���������Ϊ20%�ɵ�![]() =0.2�����a=0.75����CO��ת����Ϊ75%���ʴ�Ϊ��75%��
=0.2�����a=0.75����CO��ת����Ϊ75%���ʴ�Ϊ��75%��


 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�װ��ͼ����������ȷ���ǣ� ��
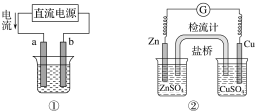
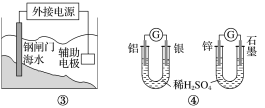
A.��ͼ��װ��ʵ�����϶�ͭ��a��Ϊͭ���������Һ������CuSO4��Һ
B.ͼ��װ��������KCl��Cl���������ձ�
C.ͼ��װ���и�բ��Ӧ����ӵ�Դ�ĸ���������ñ���
D.ͼ������װ����ͨ�����ߵĵ�������ͬʱ�����ĸ������ϵ����ʵ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F������ij����Ѫҩ���Ʊ�����ҵ����F��һ��·��ͼ���£�����H��FeCl3��Һ�ܷ�����ɫ��Ӧ����
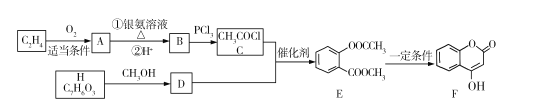
�ش��������⣺
(1)A�������� ___��E�еĹ�������������____��
(2)B��C�ķ�Ӧ������ ___��F�ķ���ʽΪ____��
(3)H�Ľṹ��ʽΪ ___��
(4)E��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ___��
(5)ͬʱ��������������D��ͬ���칹�干��____�֣�д���˴Ź���������5�������ʵĽṹ��ʽ ___
���Ƿ����廯����
������NaHCO3��Һ��Ӧ
������FeCl3��Һ����ɫ
��1mol���������Ʒ�Ӧʱ���ɵõ�1molH2
(6)��2�ȱ��ᡢ����Ϊԭ���Ʊ��۱�ϩ�ᱽ����(![]() )��д���ϳ�·��ͼ�����Լ���ѡ��_________��
)��д���ϳ�·��ͼ�����Լ���ѡ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����()
A. NaCl��Ħ��������58.5gB. 64g�����к���2mol��
C. 4g�����к���2mol��ԭ��D. 0.1molCO2�к���6.02��1022��CO2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����ֳ����л���ı���ģ��ʾ��ͼ������˵������ȷ����( )
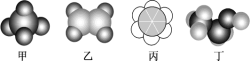
A.������黥Ϊͬϵ��
B.�ҿ�����ˮ�����ӳɷ�Ӧ��Ҳ���Ա����Ը��������Һ����
C.���е�̼̼���ǽ���̼̼������̼̼˫��֮��Ķ��صļ�
D.��(CH3CH2OH)������ϩ��ˮ����ȡ����Ӧ�Ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼�IJ�������������(CCUS)���ҹ���Դ�����һ����Ҫս�Է���CO2��ת�����л���ʵ��̼ѭ������ 2 L �ĺ��º����ܱ������У����� 2molCO2 �� 6molH2��һ�������·�����Ӧ��CO2(g)+3H2(g)CH3OH(g)+H2O(g)����� CO2 �� CH3OH(g)��Ũ����ʱ��仯��ͼ��
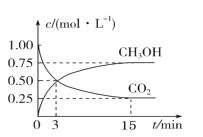
(1)�� 3 min �� 15min����(H2)=____molL��1min��1��
(2)��˵��������Ӧ�ﵽƽ��״̬����_____����)��
A. ��Ӧ�� CO2 �� CH3OH �����ʵ���Ũ��֮��Ϊ 1��1(��ͼ�н����)
B. ��������ѹǿ����ʱ��ı仯���仯
C. ��λʱ�������� 1mol H2��ͬʱ���� 1mol CH3OH
D. ��������ƽ���ܶȲ���ʱ��ı仯���仯
(3)ƽ��ʱ CO2 ��ת����Ϊ _____��
(4)ƽ���������� CO2(g)�� H2(g)�����ʵ���֮���� ______��
(5)�� 3 ����ʱ����(CH3OH)______�� 15 ����ʱ����(CH3OH)(���������������� ��=��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ֤��C2H5X��X=Cl��Br�� I���д�����ԭ�ӣ�ijͬѧ�������ʵ�飺
����C2H5X�м�����������Һ��������ã�Һ���Ϊ���㣬��Ϊ��ɫ��Һ��
����C2H5X�м�������������Һ��������ã�Һ���Ϊ���㣬��Ϊ��ɫ��Һ��
��ȡ����������
(1)��Ϊ����ʵ�飬Ŀ����_______��
(2)д�����еĻ�ѧ����ʽ��_______��
(3)��ȫ���е�ʵ�����������_______��˵��C2H5X�к���ԭ�ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������19.2��ͭ��400����ϡ���ᷢ�����·�Ӧ3Cu��8HNO3(ϡ)=3Cu(NO3)2��2NO����4H2O
(1)��˫���ű�ʾ������ת�Ƶķ������Ŀ_____________
(2)����ϡ��������ʵ���Ũ��_____________
(3)��������������ڱ���µ����_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������M���C������أ���ͼ������ԭ���á������ܶȸߵ��ŵ㣬������Ϊ����Դ�������ƶ��豸�ĵ�Դ�������طŵ���ܷ�Ӧ����ʽΪ��4M+nO2+2nH2O=4M(OH) n����֪����ص������۱�������ָ��λ�����ĵ缫�������������ͷų��������ܡ�����˵������ȷ����

A. ���ö�缫��Ŀ������ߵ缫��������Һ�ĽӴ��������������������ɢ���缫����
B. �Ƚ�Mg��Al��Zn���ֽ����C������أ�Al�C������ص����۱��������
C. M�C������طŵ���̵�������Ӧʽ��4Mn++nO2+2nH2O+4ne�C=4M(OH)n
D. ��M�C��������У�Ϊ��ֹ����������Mg(OH)2���˲������Ե���ʼ������ӽ���Ĥ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com