
【题目】研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题:
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示: 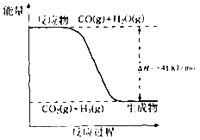
①反应的热化学方程式为 .
②已知:C(s)+H2O (g)═CO(g)+H2(g)△H=+131kJmoL﹣1
则C(s)+CO2(g)═2CO(g)△H= .
(2)化学反应可视为旧键断裂和新键形成的过程.:已知N≡N键的键能是948.9kJmol﹣1 , H﹣H键的键能是436.0kJmol﹣1;N﹣H键的键能是391.55kJ/mol..则 ![]() N2(g)+
N2(g)+ ![]() H2(g)═NH3(g)△H= .
H2(g)═NH3(g)△H= .
(3)在25℃、101Pa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
【答案】
(1)CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41kJ?mol﹣1;+172kJ/mol
(2)﹣46.2 KJ/moL
(3)CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJ?mol﹣1
O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJ?mol﹣1
【解析】解:(1)①图象分析反应是放热反应,焓变为﹣41KJ/mol,标注物质狙击状态和对应反应焓变得到热化学方程式为:CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41kJmol﹣1 , 所以答案是:CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41kJmol﹣1;②(1)CO(g)+H2O(g)═CO2(g)+H2(g)△H=﹣41kJmol﹣1;(2)C(s)+H2O(g)═CO(g)+H2(g)△H=+131kJmol﹣1
依据盖斯定律(2)﹣(1)得到:C(s)+CO2(g)═2CO(g)△H═+172kJ/mol,
所以答案是:+172kJ/mol;(2)N≡N键的键能是948.9kJmol﹣1 , H﹣H键的键能是436.0kJmol﹣1; N﹣H键的键能是391.55kJmol﹣1 . 则 ![]() N2(g)+
N2(g)+ ![]() H2(g)═NH3(g);
H2(g)═NH3(g);
△H=反应物键能总和﹣生成物键能总和= ![]() ×948.9kJmol﹣1 +
×948.9kJmol﹣1 + ![]() ×436.0kJmol﹣1 ﹣3×391.55kJmol﹣1=﹣46.2KJ/mol,
×436.0kJmol﹣1 ﹣3×391.55kJmol﹣1=﹣46.2KJ/mol,
所以答案是:﹣46.2 kj/mol;(3)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ.32g甲醇燃烧生成二氧化碳和液态水放出热量为725.76KJ;则表示甲醇燃烧热的热化学方程式为:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJmol﹣1 ,
O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJmol﹣1 ,
所以答案是:CH3OH(l)+ ![]() O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJmol﹣1 .
O2(g)=CO2(g)+2H2O(l)△H=﹣725.76kJmol﹣1 .


科目:高中化学 来源: 题型:
【题目】分类是化学学习和研究的常用手段,下列关于物质分类的正确组合是( )
酸 | 碱 | 盐 | 氧化物 | |
A | HNO3 | NaOH | NaCl | H2O |
B | HCl | CaO | Na2CO3 | NH3 |
C | H2SO4 | Ba(OH)2 | CO2 | Na2O2 |
D | H3PO4 | KOH | Al(OH)3 | BaSO4 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度时,N2与H2反应过程中能量变化的曲线如图.下列叙述正确的是( ) 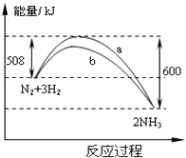
A.该反应的热化学方程式为:N2+3H22NH3△H=﹣92kJ/moL
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的放热增多
D.加入催化剂可增大正反应速率,降低逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能达到预期目的的是( )
序号 | 实验内容 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较Cl2、Br2的非金属性强弱 |
B | Cl2、S分别与Fe反应 | 比较Cl2、S的氧化性强弱 |
C | 测定相同浓度的Na2CO3、Na2SO4两溶液的pH | 比较碳酸、硫酸的稳定性强弱 |
D | 测定相同浓度的盐酸、醋酸两溶液的导电性 | 比较盐酸、醋酸的酸性强弱 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在研究合成氨方法的历史上,不同的研究者曾3次获诺贝尔化学奖。合成氨大大提高了农作物的产量,同时也是制取硝酸、炸药等的原料。下列说法中正确的是
A. N2和H2在点燃或光照条件下可合成NH3
B. NH3和HNO3溶于水后都能导电,故二者都是电解质
C. NH3遇到浓硝酸会发生反应产生大量白烟
D. 由NH3制HNO3的过程中,氮元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将aLHCl完全溶于水得到VmL盐酸,溶液的密度为ρg·cm-3,溶质的质量分数为ω,溶质的物质的量浓度为CmolL。下列叙述中错误的是
A. 可利用CCl4和水吸收HCl,且能防倒吸
B. ω=![]() ×100%
×100%
C. c= ![]() mol/L
mol/L
D. 上述溶液中再加入VmL水,所得溶液的质量分数小于0.5ω
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度不同压强(P1<P2)下,可逆反应2X(g)2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
A.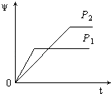
B.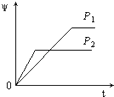
C.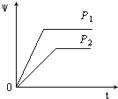
D.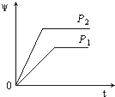
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种元素,已知:①X2﹣、Y﹣均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3 , ZY3溶液遇苯酚呈紫色.
请回答:
(1)Y的最高价氧化物对应水化物的化学式是 .
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是 . 此液体具有的性质是(填序号字母).a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体.①已知一定条件下,每1 mol该气体被O2氧化放热98.0kJ.若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为 .
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)溶液在一定条件下反应,可生成一种强酸和一种氧化物.若有1.5×6.02×1023个电子转移时,该反应的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com