
| A. | ①⑤ | B. | ①③④ | C. | ②④⑥ | D. | ⑥ |
分析 ①同周期元素随原子序数的增大,原子半径减小,具有相同电子排布的离子,原子序数的大的,半径小,阴离子的半径大于原子的半径;
②非金属性越强,气态氢化物的稳定性越强;
③非金属性越强,对应阴离子的还原性越弱;
④非金属性越强,对应单质的氧化性越强;
⑤非金属性越强,对应最高价氧化物的水化物的酸性越强;
⑥元素的非金属性越强,对应的单质的得电子能力越强.
解答 解:①同周期元素随原子序数的增大,原子半径减小,则S>Cl,阴离子的半径大于原子的半径,S2->S,所以S2->S>Cl,故①错误;
②非金属性F>Cl>S,气态氢化物的稳定性为HF>HCl>H2S,故②正确;
③非金属性Cl>Br>S,对应离子的还原性为S2->Br->Cl-,故③错误;
④非金属性Cl>S>Se,对应单质的氧化性为Cl2>S>Se,故④正确;
⑤非金属性Cl>S>Se,对应最高价氧化物的水化物的酸性为H4ClO4>H2SO4>H2SeO4,故⑤错误;
⑥非金属性F>Cl>S,非金属性越强,对应的单质的得电子能力越强,故⑥正确;
故选C.
点评 本题考查非金属元素的性质,为高频考点,明确同周期、同主族元素的性质变化规律及元素非金属性的比较方法是解答本题的关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢化物不稳定 | |
| B. | 最高价氧化物对应的水化物是一种强酸 | |
| C. | 其单质既有氧化性又有还原性 | |
| D. | 是植物生长所需要的一种营养元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
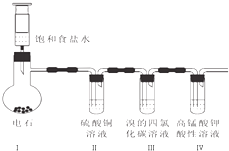 实验室制乙炔并检验其性质的装置如图.
实验室制乙炔并检验其性质的装置如图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 | B. | 32 | C. | 60 | D. | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y元素最高价氧化物对应水化物的化学式为H2YO4 | |
| B. | X与W可以形成W2X、W2X2两种化合物 | |
| C. | Z的氢化物的沸点比X的氢化物的沸点高 | |
| D. | Y、Z两元素的简单离子的半径Y>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com