
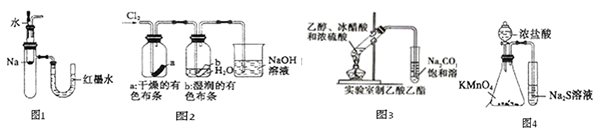
| A.图1中:将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升 |
| B.图2中:观察到湿润的有色布条能退色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成。 |
| C.图3可用于制备乙酸乙酯 |
D.图4可以比较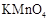 、 、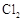 和S氧化性的相对强弱 和S氧化性的相对强弱 |


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源:不详 题型:单选题
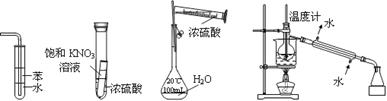
| A.实验I:可用于吸收氨气,并能防止倒吸 | B.实验Ⅱ:静置一段时间,小试管内有晶体析出 |
| C.实验III:配制一定物质的量浓度的稀硫酸 | D.实验Ⅳ:海水的淡化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 序号 | 实验操作 | 实验目的 |
| A | 浓、稀HNO3分别与Cu反应 | 比较浓、稀HNO3的氧化性强弱 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 测定等浓度的HCl、HNO3两溶液的pH | 比较Cl、N的非金属性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
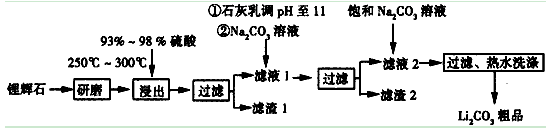
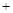 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4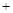 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓| T/℃ | 20 | 40 | 60 | 80 |
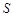 (Li2CO3)/g (Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
 (Li2SO4)/g (Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
  |  |  
|   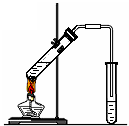  | ||
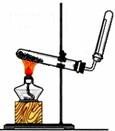
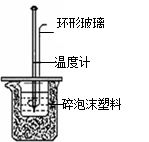
| A.实验室制取氨气 | B.配制100 mL 0.1 mol /L盐酸 | C.测定中和反应的反应热 | D.实验室制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 |
| D.用容量瓶配制一定物质的量浓度的NaOH溶液时,溶解后的溶液要马上转移至容量瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定 次数 | 待测溶液的体积 /mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com