
| A. | ⑤③①②④⑥⑦ | B. | ②③①⑤④⑦⑥ | C. | ②④①③⑦⑤⑥ | D. | ⑤③①④②⑦⑥ |
分析 先溶解光卤石,再加入沉淀剂Ca(OH)2,使Mg2+沉淀,过滤Mg(OH)2,将Mg(OH)2转化率MgCl2,电解熔融的MgCl2,制备金属Mg.
解答 解:提纯光卤石得到MgCl2的步骤为:先将光卤石溶解于水,因为KCl、MgCl2均易溶于水,故沉淀Mg2+,加入沉淀剂Ca(OH)2,使Mg2+沉淀,转化为Mg(OH)2,过滤除去KCl等,洗涤Mg(OH)2后,溶于适量的盐酸发生反应:Mg(OH)2+2HCl═MgCl2+2H2O,蒸发溶液得MgCl2•6H2O,由于加热MgCl2•6H2O的过程中,部分MgCl2发生水解:MgCl2+2H2O?Mg(OH)2+2HCl,根据平衡移动原理,在HCl气流中加热MgCl2•6H2O,使MgCl2的水解反应得到抑制,故能得到纯净的MgCl2;Mg性质活泼,只能用电解法制取.故实验顺序为②③①⑤④⑦⑥.
故选B.
点评 本题考查物质的制备以及分离、提纯,侧重考查学生的逻辑思维能力及分析问题能力,难度较大,准确率较低,注意把握实验的原理和物质的性质.


科目:高中化学 来源: 题型:选择题

| A. | 锌是负极,电子流向为“锌片→LED灯→铜片→稀H2SO4→锌片” | |
| B. | 氢离子在铜片表面被还原 | |
| C. | 如果将硫酸换成橙汁,LED 灯不能发光 | |
| D. | 该电源工作时,烧杯中阳离子向Zn极移动,且c(H+)减小,c(Cu2+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 | |
| B. | 从海水中可以得到NaCl,电解NaCl溶液可以制备Na | |
| C. | 从海水中提取溴的工艺流程中溴蒸气被吸收剂SO2吸收的目的是将海水中的溴富集 | |
| D. | 海水中提取镁所涉及的化学反应全部是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
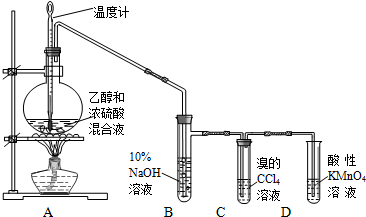 实验室制取乙烯并检验乙烯性质的装置如图.
实验室制取乙烯并检验乙烯性质的装置如图.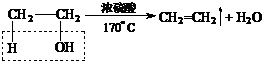 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molMg变成Mg2+时失去的电子数为NA | |
| B. | 标准状况下,22.4L氮气含有的氮原子数为NA | |
| C. | 48gO3所含氧原子数为3NA | |
| D. | 18gH2O中所含的电子数我8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9gD2O中含有的电子数为5NA | |
| B. | 1molMgCl2中含有的离子数为2NA | |
| C. | 1molCH4分子中共价键总数为4NA | |
| D. | 7.1gCl2与足量NaOH溶液反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu | B. | Fe | C. | Zn | D. | Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下镁铝表面能生成一层致密的氧化膜,保护内层的金属不被继续氧化 | |
| B. | 未打磨的铝箔因表面有氧化膜,因此在空气中加热后不能燃烧,若将氧化膜去除后再加热,则可在空气中燃烧 | |
| C. | 在化学反应中,由于铝原子能失去三个电子,而钠原子只能失去一个电子,所以铝的还原性比钠强 | |
| D. | 因铜是不活泼金属,故即使在潮湿的空气中也不会被腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com