
【题目】向含Al2(SO4)3 和 AlCl3的混合溶液中逐滴加入1 mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
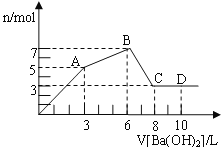
A.图中A点生成的沉淀是BaSO4和Al(OH)3
B.原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2
C.AB段反应的离子方程式为:3Ba3++2Al3++8OH-+3SO4=BaSO4↓+2AlO2-+4H2O
D.向D点溶液中通入CO2气体,立即产生白色沉淀
【答案】C
【解析】
试题分析:向含Al2(SO4)3 和 AlCl3的混合溶液与Ba(OH)2溶液反应的实质是Al3+与OH-、Ba2+与SO42-之间的离子反应,如下:Ba2++SO42-═BaSO4↓,Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═AlO2-+2H2O,假设1molAl2(SO4)3中SO42-完全被沉淀所需Ba(OH)2量为3mol,提供6molOH-,1molAl2(SO4)3中含有2molAl3+,由反应Al3++3OH-═Al(OH)3↓可知,2molAl3+完全沉淀,需要6molOH-,故:从起点到A点,可以认为是硫酸铝与氢氧化钡恰好发生反应生成硫酸钡、氢氧化铝沉淀,A点时SO42-完全沉淀,A-B为氯化铝与氢氧化钡的反应,B点时溶液中Al3+完全沉淀,产生沉淀达最大值,溶液中溶质为BaCl2,B-C为氢氧化铝与氢氧化钡反应,C点时氢氧化铝完全溶解。A、根据上述分析,A点生成的沉淀是BaSO4和Al(OH)3,故A正确;B、前3LBa(OH)2溶液与溶液中Al2(SO4)3反应,从3L-6L为Ba(OH)2溶液与溶液中AlCl3反应,二者消耗的氢氧化钡的物质的量相等为3L×1mol/L=3mol,由生成硫酸钡可知3n[Al2(SO4)3]=n[Ba(OH)2],故n[Al2(SO4)3]=1mol,由氯化铝与氢氧化钡生成氢氧化铝可知3n(AlCl3)=2[Ba(OH)2]=6mol,故n(AlCl3)=2mol,故原溶液中原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2,故B正确;C、OA段实质为硫酸铝与氢氧化钡恰好发生反应生成硫酸钡、氢氧化铝沉淀,反应离子方程式为:3Ba2++2Al3++6OH-+3SO42-=3BaSO4↓+2Al(OH)3↓,故C错误;D、D点的溶液中含有Ba2+、AlO2-,通入二氧化碳立即产生碳酸钡、氢氧化铝沉淀,故D正确;故选C。


科目:高中化学 来源: 题型:
【题目】漂白粉与漂白液可用于杀菌消毒,下列说法中正确的是
A. 漂白粉是纯净物,漂白液是混合物
B. 漂白粉的有效成分是Ca(ClO)2
C. 工业上将氯气通入澄清石灰水制取漂白粉
D. 漂白液的有效成分是Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法错误的是
A. “从沙滩到用户”,计算机芯片材料是指单质硅
B. 从海水中提取物质不都通过化学反应才能实现
C. 煤经过气化、液化等化学变化可转变为清洁燃料
D. 新型材料聚酯纤维、光导纤维都属于有机高分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
Ⅰ.(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:

①反应的热化学方程式为 。
②已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131 kJ·mol-1,
则C(s)+CO2(g)=2CO(g) ΔH= 。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;N—H键的键能是391.55 kJ·mol-1。则N2(g)+3H2(g)=2NH3(g) ΔH= 。
Ⅱ.下图是一个化学过程的示意图,回答下列问题:

(1)甲池是 装置,乙装置中电极A的名称 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中电极B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH= 。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假定元素周期表是有限的,根据已知的元素周期表的某些事实和理论可归纳出一些假说。
(1)已知元素周期表中的各周期可排元素种类如下:
周期 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
人们预测元素周期表第八周期将来也会排满,那么该周期排满后的元素种数是 。
A.18 B.32 C.50 D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有 种非金属元素,还有 种未发现。未发现的非金属元素处于 周期 族。
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法——三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置。
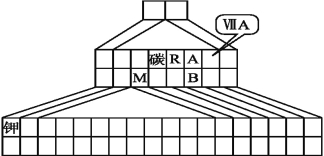
回答下列问题:
①请在图中将过渡元素所在的位置涂黑。
②画出B元素价电子排布图 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的酸性溶液中,能共存的离子组是( )
A.NH4+、NO3﹣、Al3+、Cl﹣
B.Na+、AlO2﹣、K+、NO3﹣
C.MnO4﹣、K+、SO42﹣、Na+
D.K+、SO42﹣、HCO3﹣、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,关于1.0mL0.1mol/L氨水。下列判断正确的是
A. 溶液的pH等于13
B. 加入少量NH4Cl固体,c(OH-)不变
C. c(OH-)=c(NH4+)+c(H+)
D. 与1.0mL0.1mol/L盐酸混合后,溶液呈中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com