
| A. | 主族元素分布于短周期和长周期里,而副族元素仅分布于长周期里 | |
| B. | 元素周期表中,位于同一主族的元素的原子最外层电子数相同,且等于族序数 | |
| C. | 元素周期表中,周期的序数就是该周期元素原子具有的电子层数 | |
| D. | 元素周期表有7个横行,7个周期;18个纵列,18个族 |
分析 A.主族元素由短周期和长周期组成,而副族元素均在第四周期之后;
B.主族元素的最外层电子数=族序数;
C.主族元素的周期数=电子层数;
D.元素周期表中有18个纵列,有16个族.
解答 解:A.主族元素分布于短周期和长周期里(如H、Cl、As等),而副族元素仅分布于长周期里(周期表中第3~11列),故A正确;
B.主族元素的最外层电子数=族序数,则位于同一主族的元素的原子最外层电子数相同,且等于族序数,故B正确;
C.主族元素的周期数=电子层数,则周期的序数就是该周期元素原子具有的电子层数,故C正确;
D.元素周期表有7个横行,7个周期;元素周期表中有18个纵列,有16个族,7个主族、7个副族、1个0族、1个第ⅤⅢ族,故D错误;
故选D.
点评 本题考查元素周期表的结构与应用,为高频考点,把握原子结构与元素位置的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
 ,空间构型为正四面体.
,空间构型为正四面体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C>B>A | B. | B>C>A | C. | A>B>C | D. | A>C>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=C(CH2CH3)C (CH3)3 | B. | CH2=C(CH3)C(CH3)2CH2CH3 | ||
| C. | HC≡CCH(CH3)C(CH3)3 | D. | (CH3)3CC(CH3)=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
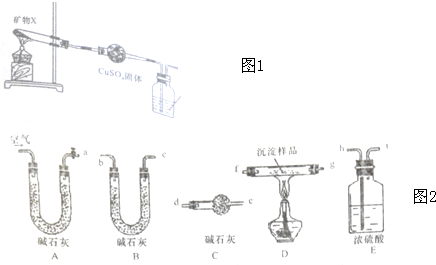
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
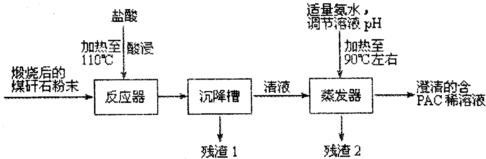
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和石灰水中加入生石灰,若保持温度不变,则pH不变 | |
| B. | 升高饱和石灰水的温度时,Ca(OH)2溶度积常数Ksp减小 | |
| C. | 饱和石灰水中加入生石灰,若保持温度不变,则溶液中Ca2+的物质的量不变 | |
| D. | 向饱和石灰水中加入浓CaCl2溶液会有Ca(OH)2沉淀析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 需加入的试剂 | 分离装置 | |
| 苯(乙醇) | ||
| 乙烷(乙烯) | ||
| 乙醇(乙酸) | ||
| 溴苯(Br2) | ||
| 苯(苯酚) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com