
| A�� | Y�ĵͼ������Z�ĵ���ˮ��Һ������Ư���ԣ�����O3Ư��ԭ����ͬ | |
| B�� | X��Z�γɵĻ������W2Y�ľ���������ͬ | |
| C�� | ��ҵ�ϳ��õ����Ӧ������Һ�Ʊ�W��X��Z�ĵ��� | |
| D�� | XԪ�ص�����Һ���ܳ����ԣ�Ҳ���ܳʼ��� |
���� W��X��Y��Z��ԭ���������������ͬһ����Ԫ�أ�W��X�ǽ���Ԫ�أ�Y��Z�Ƿǽ���Ԫ�أ�W��X���Ե��������Ӧ��ˮ������Է�Ӧ�����κ�ˮ������֪WΪNa��XΪAl��Y�������������Ǻ�����Ӳ�����2������W��Y���γɻ�����W2Y��Y����-2�ۣ���YΪS����ZΪCl���ݴ˽��
��� �⣺W��X��Y��Z��ԭ���������������ͬһ����Ԫ�أ�W��X�ǽ���Ԫ�أ�Y��Z�Ƿǽ���Ԫ�أ�W��X���Ե��������Ӧ��ˮ������Է�Ӧ�����κ�ˮ������֪WΪNa��XΪAl��Y�������������Ǻ�����Ӳ�����2������W��Y���γɻ�����W2Y��Y����-2�ۣ���YΪS����ZΪCl��
A��Y�ĵͼ�������Ϊ��������������������ˮ��Һ������Ư���ԣ���������������ɫ���ʻ���Ϊ��ɫ���ʣ���O3Ư��ԭ����ͬ�������������ǿ�����ԣ���O3Ư��ԭ����ͬ����A����
B��X��Z�γɵĻ�����ΪAlCl3�����ڷ��Ӿ��壬��Na2S�������Ӿ��壬��B����
C����ҵ�ϣ���������Ȼ��Ƶõ��ƣ������������������������������Ȼ��ƻ��Ȼ�����Һ�Ʊ���������C����
D��AlԪ�ص�����Һ���ܳ����ԣ�Ҳ���ܳʼ��ԣ����Ȼ�����Һ�����ԣ���ƫ��������Һ�ʼ��ԣ���D��ȷ��
��ѡ��D��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã���ȷ�ƶ�Ԫ���ǽⱾ��ؼ���ע������Ԫ�ػ��������ʡ������Ļ�ѧ��ҵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

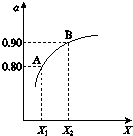

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ħ��������g/mol | B�� | ����Ħ�������mol/L | ||
| C�� | �ܽ�ȣ�g/100gH2O | D�� | �ܶȣ�g/cm3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2�ͳ���ʯ��ˮ��Ӧ��Cl2+2OH-�TCl-+ClO-+H2O | |
| B�� | NaHCO3��Һ��NaOH��Һ��Ӧ��OH-+HCO3-�TCO2��+H2O | |
| C�� | ��AlCl3��Һ�м�������İ�ˮ��Al3++3OH-�TAl��OH��3�� | |
| D�� | ʵ�����ô���ʯ��ϡ������ȡCO2��CaCO3+2H+�TCa2++CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ������Ͷ��ǿ�������Դ������Ҫ������չ���Ҵ����͡� | |
| B�� | ����ϩ��������Է����ӳɡ�ˮ���������Ӧ | |
| C�� | ���ͱ�����Ļ����1mol����ȫȼ������O2�ķ�����Ϊ7.5NA | |
| D�� | �ұ��ܱ�����KMnO4��Һ����������Ϊ�����Բ����ϵ�-CH2-������Ӱ�죬ʹ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
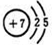 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� | 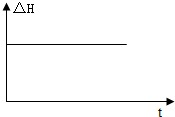 | ||
| C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
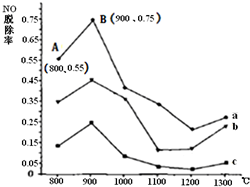 ����[CO��NH2��2]��һ������������Ч��NOת��ΪN2����ͼΪCO��NH2��2��ij����������ҪΪN2��NO����NO�����ʵ�����ֵ�ֱ�Ϊ1��2��2��1��3��1ʱ��NO�ѳ��ʣ�NO����������NO��ԭʼ���ı�ֵ�����¶ȱ仯������ͼ��
����[CO��NH2��2]��һ������������Ч��NOת��ΪN2����ͼΪCO��NH2��2��ij����������ҪΪN2��NO����NO�����ʵ�����ֵ�ֱ�Ϊ1��2��2��1��3��1ʱ��NO�ѳ��ʣ�NO����������NO��ԭʼ���ı�ֵ�����¶ȱ仯������ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com