
| A. | 对于C2H4 (g)+H2O(g)?C2H5OH(g),在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为2 mol,则用分压表示的平衡常数Kp=$\frac{3}{P}$ | |
| B. | 恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)?2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,若此时再充入3mol N2,则平衡正向移动 | |
| C. | 恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)?2C(g)达到平衡时,A、B和 C的物质的量分别为4mol、2mol和4mol,若此时A、B和C均减少1 mol,平衡逆向移动 | |
| D. | 对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关 |
分析 A.用平衡分压代替下衡浓度计算,分压=总压×物质的量分数,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为l mol计算分压,结合平衡常数K=$\frac{P({C}_{2}{H}_{5}OH)}{P({C}_{2}{H}_{4})P({H}_{2}O)}$计算判断;
B.设平衡时容器体积为1L,该温度下平衡常数K=$\frac{{1}^{2}}{1×{1}^{3}}$=1,再向容器中再充入3mol N2,利用体积之比等于气体物质的量之比计算容器体积,再计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行;
C.在容积可变的情况下,从对平衡混合物中三者的物质的量对各物质的量的浓度影响角度思考.在“均减半”或“均加培”时,相当于A、B、C三物质的浓度都没有改变,原平衡时A、B和C的物质的量之比为2:1:2,“均减少1mol”时相当于相当于在原来的基础上减少了B;
D.平衡常数随温度变化,平衡浓度计算和平衡分压计算表达意义相同.
解答 解:A.体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为l mol,分压P(C2H5OH)=P×$\frac{1}{3}$=$\frac{P}{3}$,P(C2H4)=P×$\frac{1}{3}$=$\frac{P}{3}$,P(H2O)=P×$\frac{1}{3}$=$\frac{P}{3}$,平衡常数K=$\frac{P({C}_{2}{H}_{5}OH)}{P({C}_{2}{H}_{4})P({H}_{2}O)}$=$\frac{3}{P}$,故A正确;
B.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)?2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,设平衡时容器体积为1L,该温度下平衡常数K=$\frac{{1}^{2}}{1×{1}^{3}}$=1,若此时再充入3molN2,恒温恒压下体积之比等于气体物质的量之比,则容器体积=1L×$\frac{6}{3}$=2L,Qc=$\frac{(\frac{1}{2})^{2}}{\frac{4}{2}×(\frac{1}{2})^{3}}$=1=K,平衡不动,故B错误;
C.在容积可变的情况下,从对平衡混合物中三者的物质的量对各物质的量的浓度影响角度思考.在“均减半”或“均加培”时,相当于A、B、C三物质的浓度都没有改变,原平衡时A、B和C的物质的量之比为2:1:2,“均减少1mol”时相当于相当于在原来的基础上减少了B,平衡逆向移动,故C正确;
D.平衡常数随温度变化,平衡浓度计算和平衡分压计算表达意义相同,对于一定条件下的某一可逆反应,用平衡浓度表示的甲衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关,故D正确;
故选B.
点评 本题考查了化学平衡常数的表达意义,为高频考点,侧重于学生的分析、计算能力的考查,影响化学平衡的因素分析,注意化学平衡移动原理的应用和容器特征的分析判断,题目难度中等.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
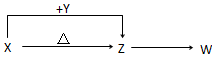 X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.
X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.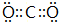 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
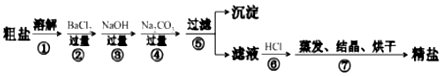
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO3与H2O2的反应为氧化还原反应 | |
| B. | 因为SO2有漂白性,所以SO2可使溴水褪色 | |
| C. | 50 mL 18.4 mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/ (mol•L-1) | 0.44 | 0.6 | 0.6 |
| 化学键 | N≡N | F-F | N-F |
| 键能/kJ•mol-1 | 941.7 | 154.8 | 283.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
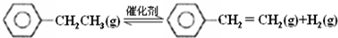
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com