
实验室欲用氯化钠固体配制500mL、0.10mol·L-1的NaCl溶液,下列叙述正确的是( )
A.实验用到的仪器有:托盘天平、烧杯、1000mL容量瓶、玻璃棒
B.将称量好的固体放入500mL容量瓶中溶解
C.定容时若俯视刻度,则所得溶液浓度偏高
D.定容后翻转摇匀,发现液面下降,又加入蒸馏水到刻度线
科目:高中化学 来源: 题型:
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
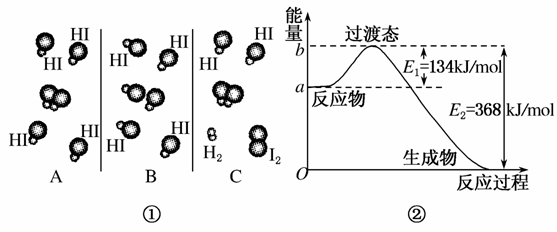
(1)图①是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”)。
(2)20世纪30年代Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。图②是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________
______________________________________________________________。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图②中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O===O | P===O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
已知白磷的燃烧热为2 378.0 kJ/mol,白磷完全燃烧的产物结构如图③所示,则上表中x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是
A. 高纯度的硅广泛用于制作计算机
B. 硅可由二氧化硅还原制得
C. 低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D. 自然界中硅的储量丰富,自然界中存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
| 氧化物 | 环境问题 | 主要来源 | |
| A | CO | 煤气中毒 | 含碳燃料的不完全燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO2 | 酸雨 | 化石燃料的燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数,下列说法正确的是( )
A.0.2 mol H2O2完全分解转移的电子数为0.4NA
B.含NA个Na+的Na2O溶于1L水中,Na+的物质的量浓度为1mol·L-1
C.在标准状况下,2.8g N2和2.24LCO所含电子数均为1.4NA
D. 2.24L SO2与O2混合气体中所含氧原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
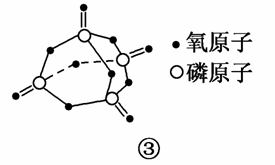
A.碳酸氢镁溶液加入过量氢氧化钠: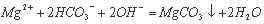
B.碳酸钡溶于醋酸溶液: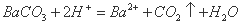
C.次氯酸钙溶液中通入少量二氧化碳: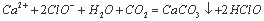
D.氧化铁加入氢碘酸中: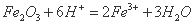
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.某溶液中加入Ba( NO3)2溶液和稀盐酸(过量)析出白色沉淀,则溶液中一定含SO42一.
B.硫酸加入漂白粉中能生成氯气,可用排饱和食盐水法收集
C.NaOH溶液不能保存在带胶头滴管的试剂瓶中,因为NaOH与磨口处的SiO2反应生成Na2SiO3形成粘结
D.可用热的饱和碳酸钠溶液除去金属表面的植物油
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z中,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X2+的氧化性小于Y3+的氧化性。下列说法正确的是( )
A.X、Y、Z、W的原子半径依次增大
B.W与Z一定具有相同的最高正化合价
C.W的最高价氧化物的水化物一定是强酸
D.以X、Y、硫酸铜溶液组成的原电池中,Y作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

请回答下列问题:
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是____________________________;
(2)图中ΔH=________kJ·mol-1;
(3)V2O5的催化循环机 理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:_____________________________________________;
理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:_____________________________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH(要求计算过程)。(已知燃烧热是指25 ℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com